硫酸铵是常用的一种氮肥,现有一种硫酸铵化肥,为测定其中硫酸铵的质量分数, 采用如图(甲)所示的装置进行实验。已知在A、B中所发生反应的化学方程式如下:(NH4)2SO4+2NaOH=====2NH3↑+2H2O+ Na2SO4 2NH3+H2SO4====(NH4)2SO4(注:反应生成的NH3能被烧杯中的稀硫酸溶液完全吸收)
采用如图(甲)所示的装置进行实验。已知在A、B中所发生反应的化学方程式如下:(NH4)2SO4+2NaOH=====2NH3↑+2H2O+ Na2SO4 2NH3+H2SO4====(NH4)2SO4(注:反应生成的NH3能被烧杯中的稀硫酸溶液完全吸收)
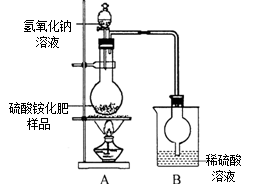
(1)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是 。
(2)方案评价:根据右图实验设计测得的数据,计算出硫酸铵的质量分数可能偏高,因为实验装置的设计存在一个明显缺陷 。
(3)现称取27g硫酸铵化肥样品,用改进后的实验装置重新进行实验,实验后测得B装置的质量增加了6.8g。请通过计算确定该化肥中硫酸铵的质量分数。(计算结果准确到0.1%)








 粤公网安备 44130202000953号
粤公网安备 44130202000953号