采用N 2O 5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用,回答下列问题:
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N 2O 5 , 该反应的氧化产物是一种气体,其分子式为________。
(2)F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N 2O 5(g)分解反应:
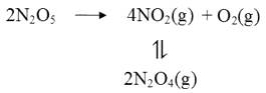
其中NO 2二聚为N 2O 4的反应可以迅速达到平衡,体系的总压强p随时间t的变化如下表所示(t=x时,N 2O 4(g)完全分解):
t/min |
0 |
40 |
80 |
160 |
260 |
1300 |
1700 |
∞ |
P/kPa |
35.8 |
40.3 |
42.5 |
45.9 |
49.2 |
61.2 |
62.3 |
63.1 |
①已知:2N 2O 5(g)=2N 2O 4(g)+O 2(g) △H 1=-4.4kJ·mol -1
2NO 2(g)=N 2O 4(g) △H 2=-55.3kJ·mol -1
则反应N 2O 5(g)=2NO 2(g)+ O 2(g)的△H=________ kJ·mol -1
②研究表明,N 2O 5(g)分解的反应速率v=2×10 -3× (KPa·min -1),t=62min时,测得体系中 =2.9kPa,则此时的 =________ kPa,V=________ kPa,min -1。
③若提高反应温度至35℃,则N 2O 5(g)完全分解后体系压强p X(35℃)________63.1kPa(填"大于""等于"或"小于"),原因是________。
④25℃时N 2O 4(g) ⇋2NO 2(g)反应的平衡常数K p=________ kPa (K p为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N 2O 5(g)→4NO 2(g)+O 2(g),R,A,Ogg提出如下反应历程:
第一步N 2O 5⇋NO 3+NO 2快速平衡
第二步NO 2+NO 3⇀NO+NO 2+O 2 慢反应
第三步NO+NO 3⇀2NO 2快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是 __________(填标号)。
| A. |
ν(第一步的逆反应P>ν(第二步反应) |
| B. |
反应的中间产物只有NO 3 |
| C. |
第二步中NO 2与NO 3的碰撞仅部分有效 |
| D. |
第三步反应活化能较高。 |








 粤公网安备 44130202000953号
粤公网安备 44130202000953号