Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻,能量密度大等优良性能,得到广泛应用,回答下列问题:
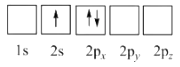
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为________、________。(填标号)
| A. |
|
| B. |
|
| C. |
|
| D. |
|
(2)Li +与H -具有相同的电子构型,r(Li +)小于r(H -),原因是________。
(3)LiAlH 4是有机合成中常用的还原剂,LiAlH 4中的阴离子空间构型是________。中心原子的杂化形式为________,LiAlH 4中,存在________(填标号)。
| A. |
离子键 |
| B. |
σ键 |
| C. |
π键 |
| D. |
氢键 |
(4)Li 2O是离子晶体,其晶格能可通过图(a)的 Born-Haber循环计算得到
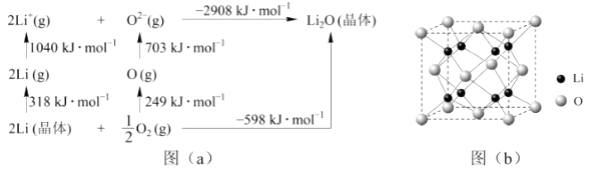
可知,Li原子的第一电离能为________kJ·mol -1 , O=O键键能为________kJ·mol -1 , Li 2O晶格能为________kJ·mol -1
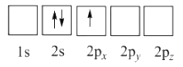
(5)Li 2O具有反莹石结构,晶胞如图(b)所示。已知晶胞参数为0.4665mm,阿
伏加德罗常数的值为N A,则Li 2O的密度为 ________ g/cm 3(列出计算式)。










 粤公网安备 44130202000953号
粤公网安备 44130202000953号