下列离子方程式书写正确的是
| A.氯气溶于水:Cl2+H2O═2H++Cl﹣+C1O﹣ |
| B.溴化钠溶液与氯气反应:2Br﹣+Cl2═2Cl﹣+Br2 |
| C.氢氧化钡溶液与稀硫酸反应:H++SO42﹣+Ba2++OH﹣═H2O+BaSO42﹣↓ |
| D.碳酸钙加入过量的盐酸中:CO32﹣+2H+═CO2↑+H2O |
下列物质间的转化,通过一步反应不能实现的是
| A.CO2→Na2CO3 | B.FeCl3→FeCl2 |
| C.H2SiO3→Na2SiO3 | D.S→SO3 |
工业上可通过反应2Al2O3+3C+6Cl2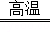 AlCl3+3CO2制取无水氯化铝,下列有关该反应的说法正确的是
AlCl3+3CO2制取无水氯化铝,下列有关该反应的说法正确的是
| A.Cl2是氧化剂 | B.Al2O3是还原剂 |
| C.C发生还原反应 | D.氧原子得到电子 |
下列实验方法不正确的是
| A.用BaCl2溶液鉴别硫酸铵和氯化铵两种固体 |
| B.用尝味道的方法鉴别蔗糖溶液和硫酸溶液 |
| C.用稀盐酸鉴别碳酸钾和硝酸钾两种固体 |
| D.用灼烧闻气味的方法鉴别丝绸和棉布 |
下列有关物质用途的说法不正确的是
| A.碳铵与碱性肥料混合施用.以提高肥效 |
| B.用氧化铝制造耐火材料 |
| C.在医疗上,可用碳酸氢钠治疗胃酸过多 |
| D.用硫酸钡制作白色颜料 |
下列关于0.2mol/L Ba(NO3)2溶液的说法中,正确的是
| A.溶液中含有的阴、阳离子总数为0.6mol |
| B.在0.5 L该溶液中,Ba2+的浓度为0.1 moI/L |
| C.在500 mL该溶液中,含有0.2molNO3﹣ |
| D.取1L该溶液稀释到10L时,NO3﹣的浓度为0.02 mol/L |
碘元素的一种核素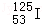 可用于治疗肿瘤.下列有关
可用于治疗肿瘤.下列有关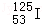 的说法正确的是
的说法正确的是
| A.质量数是53 | B.质子数是125 | C.中子数是125 | D.电子数是53 |
我国是世界上缺铁性贫血发生率较高的国家之一,2004年我国政府就已经启动了铁强化酱油项目,推广铁强化酱油.这里的铁是指
| A.元素 | B.单质 | C.原子 | D.分子 |
下列离子方程式书写不正确的是
| A.硫酸铜溶液和氢氧化钠溶液反应:Cu2﹣+2OH﹣═Cu(OH)2↓ |
| B.盐酸和氢氧化钠溶液反应:H++OH﹣═H2O |
| C.碳酸钙和盐酸溶液:CO32﹣+2H+═H2O+CO2↑ |
| D.氢氧化钡和硫酸的反应:Ba2++2OH﹣+2H++SO42﹣═2H2O+BaSO4↓ |
以下说法错误的是
| A |
2Na+2H2O=2NaOH+H2↑ 2Al+2H2O+2NaOH=2NaAlO2+3H2↑ |
均为水做氧化剂的氧化还原反应 |
| B |
Fe+CuSO4=FeSO4+Cu 2Mg+CO2=2MgO+C |
均为固体质量增大的置换反应 |
| C |
NaAlO2+SO2+2H2O=Al(OH)3+NaHSO3 NaClO+CO2+H2O=HClO+NaHCO3 |
均为较强酸制较弱酸的复分解反应 |
| D |
H2O2+SO2=H2SO4 CaO+SO3=CaSO4 |
均为非氧化还原反应的化合反应 |
A.A B.B C.C D.D
为了除去粗盐中的 Ca2+、Mg2+、SO42﹣及泥沙,可将粗盐溶于水,然后进行下列五项操作,其中正确的操作顺序是
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量 Na2CO3溶液 ⑤加过量 BaCl2溶液.
| A.①④②⑤③ | B.④①②⑤③ | C.②④⑤①③ | D.⑤②④①③ |
某兴趣小组对铜与浓硫酸反应产生的黑色沉淀(可能含有CuO、CuS、Cu2S,其中CuS和 Cu2S不溶于稀盐酸、稀硫酸)进行探究,实验步骤如下:
Ⅰ.将光亮铜丝插人浓硫酸,加热;
Ⅱ.待产生大量黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用.
回答下列问题:
(1)步骤Ⅱ产生气体的化学式为 .
(2)向含微量 Cu2+试液中滴加K4[Fe(CN)6]溶液,能产生红褐色沉淀.现将少量黑色沉淀放入稀硫酸中,充分振荡以后,再滴加K4[Fe(CN)6]溶液,未见红褐色沉淀,由此所得结论是 .
(3)为证明黑色沉淀含有铜的硫化物,进行如下实验:
| 装置 |
现象 |
结论及解释 |
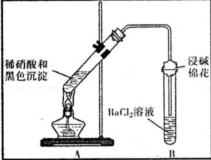 |
①A试管中黑色沉淀逐渐溶解 ②A试管上方出现红棕色气体 ③B试管中出现白色沉淀 |
a.现象②说明褐色沉淀具有 性. b.试管B中产生白色沉淀的总反应的离子方程式为 |
(4)CuS固体能溶于热的浓硫酸,请用有关平衡移动原理加以解释: .
(5)为测定黑色沉淀中Cu2S 的百分含量,取0.2g 步骤Ⅰ所得黑色沉淀,在酸性溶液中用 40.0mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4﹣+5Cu2S+44H+═10Cu2++5SO2↑+8Mn2++22H2O
6MnO4﹣+5CuS+28H+═5Cu2++5SO2↑+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,过量的高锰酸钾溶液恰好与35.0mL 0.1mol/L (NH4)2Fe(SO4)2溶液反应完全.则混合物中Cu2S 的质量分数为 .
下列叙述正确的是
| A.Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱 |
| B.漂白粉和明矾都常用于自来水的处理,二者的作用原理不相同 |
| C.将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀 |
| D.向FeCl2溶液中通入Cl2反应的离子方程式为:Fe2++Cl2═Fe3++2C1﹣ |
某非金属元素R的氢化物及其氧化物、盐之间具有如下转化关系(部分产物省略):氢化物 B
B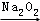 C,下列判断中正确的是
C,下列判断中正确的是
| A.若R是硫元素、则C是Na2SO3 | B.若R是硅元素、则C是Na2Si03 |
| C.若R是碳元素、则C是Na2CO3 | D.若R是氯元素、则C是NaCl |
试题篮
()