已知I2+SO32-+H2O===SO42-+2I-+2H+。某无色溶液中只可能含有I-,NH4+,Ba2+, SO32-,MnO4-中的一种或几种,若向该溶液中滴加少量的溴水,溶液仍为无色,下列判断正确的是
| A.该溶液中肯定不含I- | B.该溶液中可能含有Ba2+ |
| C.该溶液中肯定含有NH4+ | D.该溶液中可能含有MnO4- |
①2NaBrO3+Cl2====Br2+2NaClO3 ②HClO3+5HCl====3Cl2+3H2O
③2FeCl3+2KI====2FeCl2+I2+2KCl ④2FeCl2+Cl2====2FeCl3
根据上述氧化还原反应判断,氧化性由强到弱的顺序是
| A.NaBrO3>HClO3>Cl2>FeCl3>I2 |
| B.Cl2>FeCl3>I2>HClO3>NaBrO3 |
| C.I2>FeCl3>Cl2>HClO3>NaBrO3 |
| D.HClO3>NaBrO3>FeCl3>Cl2>I2 |
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是
①I2 + SO2 + 2H2O = H2SO4 + 2HI
②2FeCl2 + Cl2 = 2FeCl3
③2FeCl3 + 2HI = 2FeCl2 + 2HCl+I2
| A.SO2>I->Fe2+>Cl- | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.I->Fe2+>Cl->SO2 |
漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸(HClO2为弱酸)不稳定可分解,反应的离子方程式为:5HClO2=4ClO2↑+H++Cl-+2H2O。向NaClO2溶液中滴加H2SO4,开始时HClO2分解反应反应缓慢,随后反应迅速,其原因是
| A.在酸性条件下,亚氯酸钠的氧化性增强 |
| B.溶液中的Cl-起催化作用 |
| C.ClO2逸出,使反应的生成物浓度降低 |
| D.溶液中的H+起催化作用 |
根据下列实验现象,所得结论正确的是
| 实验 |
实验现象 |
结论 |
| A |
左边烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 |
还原性: Al>Mg>Cu |
| B |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
| C |
试管中白色固体先变淡黄色,后变为黄色 |
沉淀转化的实质就是沉淀溶解平衡的移动 |
| D |
锥形瓶中有气体产生,烧杯中溶液变浑浊 |
非金属性:Cl>C>Si |
某溶液中含有的溶质是FeBr2、FeI2 ,若先向该溶液中通人一定量的氧气.再向反应后的溶液中滴加KSCN溶液,溶液变为红色,则下列叙述正确的是
①原溶液中的Br-一定被氧化;
②通人氮气之后原溶液中的Fe2+一定有部分或全部被氧化;
③不能确定通入氯气后的落液中是否存在;
④若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的I-、Fe2+、Br-均被完全氧化
A.①②③ B.②③④ C.①③④ D①②③④。
9.下列实验现象及相关的离子方程式均正确的是
| A.Cl2与FeI2溶液反应,当n(C12):n(FeI2)=1:1时:2Fe2++2I-+2C12 |
| B.向Ba(NO3)2溶液中通人SO2气体,出现白色沉淀:Ba2++SO2+ H2O |
| C.向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2 MnO4+7 H2 O2+6 H+ |
D.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合:Ba2++SO +H++OH- +H++OH- |
现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;②2BrO3- +I2 = 2IO3-+ Br2;
请回答下列问题:
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为 ,还原产物是 。
(2)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式 。
(3)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确,并说明理由 。
(4)含6 mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为 。
(5)加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。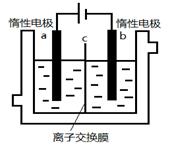
先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。阳极的电极反应式为 。
(12分)根据下图所示的关系,确定A、B、C、D、E、F的化学式,并写有关方程式。
(1)已知A为单质,则A为 (填化学式,下同),E为 。
(2)D→E的化学方程式为___________________________________。
(3)取少量C溶于水,加入酸化的硝酸银溶液,有白 色沉淀生成,则A→C的化学方程式为_____________________________。
(4)某学习小组设计如下装置进行相关实验:
①打开活塞b,向溶液B中逐滴加入少量溴水,关闭活塞b;
②打开活塞a,向容器中滴入足量的亚硫酸。
按要求回答下列问题:
①滴入溴水时,溶液的颜色变为棕黄色,该反应的离子方程式为________。
②滴入亚硫酸时,溶液由棕黄色变为浅绿色,该反应的离子方程式为______。
③由此可知,B中的阳离子、Br-、H2SO3还原性由强到弱的顺序是___________(B中的阳离子用离子符号表示)。
铋(Bi)位于元素周期表中ⅤA族,其价态为+3价较稳定,铋酸钠(NaBiO3)溶液呈无色,取一定量的硫酸锰(MnSO4)溶液依次滴加下列溶液,对应的现象如下表所示:
| 加入溶液 |
①适量铋酸钠溶液 |
②过量的双氧水 |
③适量KI淀粉溶液 |
| 实验现象 |
溶液呈紫红色 |
紫红色消失,产生气泡 |
溶液变成蓝色 |
关于NaBiO3、KMnO4、I2、H2O2的氧化性由强到弱的顺序为
A.I2、H2O2、KMnO4、NaBiO3 B.H2O2、I2、NaBiO3、KMnO4
C.NaBiO3、KMnO4、H2O2、I2 D.KMnO4、NaBiO3、I2、H2O2
稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易被氧化变暗,且受热易燃烧,遇水很快反应。下列说法正确的是(已知:铈常见的化合价有+3和+4,氧化性:Ce4+>Fe3+)
| A.电解熔融CeO2制Ce时,铈在阳极获得 |
| B.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑ |
| C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+ |
D.Ce有四种稳定的核素嚣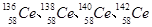 ,它们互称为同位素 ,它们互称为同位素 |
金属铈(稀土元素)性质活泼。铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2。下列说法正确的是
| A.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI ="=" CeI4 + 2H2↑ |
| B.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + Fe2+ = Ce3+ + Fe3+ |
| C.在一定条件下,电解熔融状态的CeO2制Ce,在阳极获得铈 |
D.四种铈的核素 Ce、 Ce、 Ce、 Ce、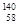 Ce、 Ce、 Ce,它们互称为同素异形体 Ce,它们互称为同素异形体 |
已知氧化性:Cl2> Fe3+ >I2。向FeI2溶液中加入一定量的氯水,有关离子方程式错误的是
| A.2 I-+ Cl2 →I2 + 2Cl- |
| B.2Fe2+ + 2I-+ 2Cl2 → 2Fe3+ + I2 + 4Cl- |
| C.2Fe2+ + 4I-+ 3Cl2 → 2Fe3+ + 2I2 + 6Cl- |
| D.2Fe2+ + 6I-+ 4Cl2 → 2Fe3+ + 3I2 + 8Cl- |
(14分)NaClO具有强氧化性,其溶液可用于游泳池及环境消毒。
(1)已知:
①Cl2(g)+2NaOH(aq)=NaCl(aq)+NaClO(aq)+H2O(l) △H=-101.1kJ·mol-1
②3NaClO(aq)=2NaCl(aq)+NaClO3(aq) △H=-112.2kJ·mol-1
则3Cl2(g)+6NaOH(aq)=5NaCl(aq)+NaClO3(aq)+3H2O(l) △H=
(2)工业上可用石墨电极电解饱和氯化钠溶液制取次氯酸钠溶液装置如图所示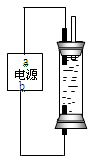
①电源中,a电极名称是
②用此装置电解热的氯化钠溶液时会有部分氯酸钠生成,若电解消耗了117g氯化钠时,电路中共转移的电子为8mol,则次氯酸钠的产率为
(3)向次氯酸钠溶液通入少量的CO2,只生成次氯酸钠和碳酸氢钠,则相同温度下,等物质的量浓度的Na2CO3、NaClO、NaHCO3溶液的pH由大到小的顺序为 。
(4)向盛有硫酸酸化的淀粉KI溶液的试管中,滴加少量次氯酸钠溶液,会立即观察到溶液变成蓝色,该反应的离子方程式为 。再向上述的蓝色溶液中,继续滴加Na2SO3溶液,又发现蓝色溶液逐渐褪色,该反应的化学方程式为 。对比上述两组实验所得结果,比较ClO― 、I2、SO42― 三种微粒氧化性由强到弱的顺序 。
试题篮
()