航天技术测得三氧化二碳(C2O3)是金星大气层的成份之一,下列关于C2O3的说法中错误的是
| A.C2O3与CO2都是碳的氧化物 | B.C2O3与CO2都是碳酸的酸酐 |
| C.C2O3与CO都具有还原性 | D.C2O3与C的燃烧产物都是CO2 |
根据下列反应判断有关物质还原性由强到弱的顺序是
H2SO3+I2+H2O===2HI+H2SO4
2FeCl3+2HI===2FeCl2+2HCl+I2
3FeCl2+4HNO3===2FeCl3+NO↑+2H2O+Fe(NO3)3
| A.H2SO3>I->Fe2+>NO | B.I->Fe2+>H2SO3>NO |
| C.Fe2+>I->H2SO3>NO | D.NO>Fe2+>H2SO3>I- |
下列物质既具有氧化性又有还原性的是( )
①SO2 ②Fe3+ ③ Fe2+ ④ HCl ⑤ H2O2
| A.①②③ | B.①③ | C.①③⑤ | D.①③④⑤ |
下列应用不涉及氧化还原反应的是
| A.Na2O2用作呼吸面具的供氧剂 | B.工业和生活中常用HF来刻蚀玻璃 |
| C.工业上利用合成氨实现人工固氮 | D.工业上电解熔融状态Al2O3制备Al |
将0.03 mol Cl2缓缓通入含0.02mol H2SO3和0.02 mol HBr的混合溶液中,在此过程溶液的c(H+)与Cl2用量的关系示意图是(溶液的体积视为不变)( )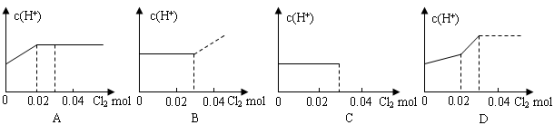
根据反应式:①2Fe3+ + 2I- = 2Fe2+ + I2 ②Br2 + 2Fe2+ ="==" 2Fe3+ +2Br-,可判断离子的还原性从强到弱的顺序是
| A.Br-、Fe2+、I- | B.I-、Fe2+、Br- |
| C.Br-、I-、Fe2+ | D.Fe2+、I-、Br- |
根据反应(1)~(4),可以判断下列四种物质的氧化性由强到弱的正确顺序
(1)Cl2+2KI===2KCl+I2 (2)2FeCl2+Cl2===2FeCl3
(3)2FeCl3+2HI===2FeCl2+2HCl+I2 (4)H2S+I2=2HI+S
| A.H2S>I2>Fe3+>Cl2 | B.Cl2>Fe3+>I2>H2S |
| C.Fe3+>Cl2>H2S>I2 | D.Cl2>I2>Fe3+>H2S |
CaH2常作为生氢剂,其中氢元素呈-1价,其化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑,其中水是( )
| A.还原剂 | B.氧化剂 |
| C.既是还原剂又是氧化剂 | D.既不是氧化剂又不是还原剂 |
已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2氧化性依次减弱,下列反应在水溶液中不可能发生的是( )
| A.3Cl2+6FeI2=2FeCl3+4FeI3 |
| B.Cl2+2FeI2=FeCl2+I2 |
| C.Co2O3+6HCl=CoCl3+Cl2↑+3H2O |
| D.2Fe3++2I-=2Fe2++I2 |
已知反应①2BrO3- + Cl2 =Br2 +2ClO3-②5Cl2 + I2 +6H2O=2HIO3 +10HCl
③ClO3- +5Cl-+6H+=3Cl2 +3H2O,下列物质氧化能力强弱顺序正确的是( )
| A.ClO3->BrO3->IO3->Cl2 | B.BrO3->Cl2>C1O3->IO3- |
| C.BrO3->ClO3->Cl2>IO3- | D.Cl2>BrO3->C1O3->IO3- |
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是
I2+SO2+2H2O H2SO4+2HI 2FeCl2+Cl2
H2SO4+2HI 2FeCl2+Cl2 2FeCl3
2FeCl3
2FeCl3+2HI 2FeCl2+2HCl+I2
2FeCl2+2HCl+I2
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |
在反应 3S + 6NaOH  2Na2S + Na2SO3 + 3H2O 中被氧化的硫与被还原的硫的关系是 ( )
2Na2S + Na2SO3 + 3H2O 中被氧化的硫与被还原的硫的关系是 ( )
| A.物质的量之比为2∶1 | B.质量比为2∶1 |
| C.质量比为 1∶2 | D.物质的量之比为1∶1 |
下列关于硫酸性质的描述中,正确的是
| A.浓H2SO4有氧化性,稀H2SO4无氧化性 |
| B.由于浓H2SO4具有吸水性,故可用来与蔗糖反应做“黑面包”实验 |
| C.稀H2SO4与铁、铝反应,浓H2SO4在常温下不与铁、铝反应 |
| D.浓硫酸与Cu的反应中有少量黑色固体生成,可能是CuO |
试题篮
()