某烃的结构简式为CH3—CH2—CH=C(C2H5)—C ≡CH,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,一定在同一平面内的碳原子数为c,则a、b、c分别为
| A.4、3、6 | B.4、3、5 | C.2、5、4 | D.4、6、4 |
现有Wg某不饱和链烃R(R分子中只含单键和双键),R能与VL(标准状况)氢气恰好完全反应,生成烷烃。若R的相对分子质量为M,阿伏加德罗常数为NA,则lmol R中含有双键数目为
| A.WVNA/22.4M | B.MVNA/22.4W |
| C.WV/22.4M | D.MV/22.4W |
提示下列信息
某无支链的环状一氯代烃A(分子式为C6H11Cl)可发生如下转化关系:
试回答下列问题:
(1)A的结构简式为__________,
(2)指出下列转化的反应类型:C→D: ________________________
(3)写出D→E的化学方程式:___________________________________________
(4)A的链状同分异构体有多种。各写出符合下列条件的一种同分异构体的结构简式。
①只有一个甲基:__________;②有3个甲基,但不存在顺反异构体:_________。
甲、乙、丙三种物质均由短周期元素组成,一定条件下,存在下列转化关系:甲+乙→丙+H20
(1)若丙为Na2C03,反应的化学方程式为 (任写一个)。 溶液中,所含的离子按物质的量浓度由大到小的顺序排列为 。
溶液中,所含的离子按物质的量浓度由大到小的顺序排列为 。
(2)若甲是石油裂解气的主要成分之一,乙为O2,且甲分子和乙分子具有相同的电子数。25℃、101 kPa时,1g甲完全燃烧生成CO2气体与液态水,放出50.5 kJ的热量,该反应的热化学方程式为 ;利用该反应设计的燃料电池中,通入甲的电极为电池的 (填“正极”或“负极”)。
(3)若甲、乙是同主族元素的化合物,丙为单质。
①丙所含元素在元素周期表中的位置为 ;
②甲与水相比,热稳定性较强的是 (填化学式)。
(共8分)实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用下图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
(1)写出实验室制备乙烯反应的化学方程式: ,实验中,混合浓硫酸与乙醇的方法是将_____________慢慢加入另一种物质中;加热F装置时必须使液体温度___________(选填缓慢或迅速)升高到170℃,圆底烧瓶中加入几粒碎瓷片的作用是 。
(2)为实现上述实验目的,装置的连接顺序为F→______________→D。(各装置限用一次)
(3)当C中观察到 时,表明单质溴能与乙烯反应;若D中 ,表明C中发生的是取代反应;若D没有出现前面所描述的现象时,表明C中发生的是加成反应。
化学反应的实质是旧键的断裂和新键的生成,在探讨发生反应的分子中化学键在何处断裂的问题时,近代科技常用同位素示踪原子法。如有下列反应:
可以推知,化合物 应时断裂的化学键应是
应时断裂的化学键应是
| A.①③ | B.①④ | C.② | D.②③ |
已知反应①:
化合物Ⅱ可由化合物Ⅰ制备,路线如下;
(1)化合物Ⅲ的化学式为 ,l mol化合物Ⅲ最多能与_____mol H2发生加成反应。
(2)写出转化Ⅳ→V的化学方程式 (注明条件)。
(3)化合物Ⅲ有多种同分异构体,其中符合下列条件的异构体有 种,写出其中任意一种的结构简式: 。
①遇FeCl3溶液显紫色;
②在浓硫酸催化作用下能发生消去反应。
(4)化合物V和化合物Ⅵ在一定条件下按物质的量m︰n反应合成高分子化台物Ⅶ,且原子转化率为100%。高分子化合物Ⅶ的结构简式为 。
(5) 能与CH2=CHCOOH发生类似反应①的反应,生成化合物Ⅷ,写出Ⅷ的一种结构简式为 。
能与CH2=CHCOOH发生类似反应①的反应,生成化合物Ⅷ,写出Ⅷ的一种结构简式为 。
(14分)某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号) 。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。
①A的结构简式为 ;
②链烃A与溴的CCl4溶液反应生成B;B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学方程式: ;
③B与足量NaOH水溶液完全反应,生成有机物E,该反应的化学方程式: ;E与乙二醇的关系是 。
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3∶2∶1,则A的名称为 。
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为 。
Ⅰ.① H与
H与 H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷
H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷 ;④甲烷(CH4)与丙烷(C3H8)。
;④甲烷(CH4)与丙烷(C3H8)。
(1)互为同位素的是______(填序号,下同)。
(2)互为同系物的是______。
(3)互为同分异构体的是______。
(4)互为同素异形体的是______。
II.A~E等几种烃分子的球棍模型如下图所示,据此回答下列问题。
(1)D的化学式为__________________,A的二氯取代物有____________种。
(2)可作为植物生长调节剂的是________________________(填序号)。
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式____________,结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)已知 2CH3CHO+O2 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
反应②的化学方程式为____________________________________。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____________________________,反应类型是__________________。
某烃的结构简式为 ,有关其分子结构的叙述中正确的是
,有关其分子结构的叙述中正确的是
| A.分子中一定在同一平面上的碳原子数为6 |
| B.分子中一定在同一平面上的碳原子数为7 |
| C.分子中在同一直线上的碳原子数为6 |
| D.分子中在同一直线上的碳原子数为4 |
某石油化工产品X的转化关系如下图,下列判断错误的是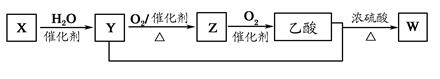
| A.X可以发生加聚反应 | B.Z与CH3OCH3互为同分异构体 |
| C.Y能与钠反应产生氢气 | D.W的结构简式为CH3COOC2H5 |
已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。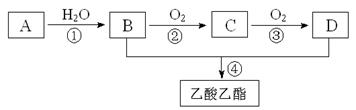
回答下列问题:
(1)写出A的电子式___________。
(2)B、D分子中的官能团名称分别___________、___________。
(3)写出下列反应的反应类型:①___________,②___________,④___________。
(4)写出下列反应的化学方程式:
① 。
② 。
④ 。
(10分)丁子香酚可用作杀虫剂和防腐剂,其结构简式如图:
(1)写出丁子香酚的分子式__________,其含氧官能团名称为__________。
(2)下列物质不能与丁子香酚发生反应的是______(填序号)。
a.NaOH溶液 b.NaHCO3溶液
c.Br2的四氯化碳溶液 d.乙醇
(3)符合下述条件的丁子香酚的同分异构体共有______种,请写出其中任意两种的结构简式______。
①与NaHCO3溶液反应
②苯环上只有两个取代基
③苯环上的一氯取代物只有两种.
试题篮
()