下列各组物质中,含有离子键的是
| A.H2 | B.NaCl | C.HCl | D.CO2 |
下列有关硫元素及其化合物的表示正确的是
A.中子数为18的硫原子: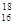 S S |
B.CS2分子的电子式: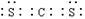 |
C.硫离子(S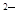 )的结构示意图: )的结构示意图: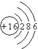 |
D.苯磺酸的结构简式: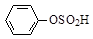 |
最近美国宇航局的科研人员确认火星地表含有溶有高氯酸盐的液态水。下列有关水及高氯酸盐的说法错误的是
| A.水是一种弱电解质 |
| B.NH4ClO4溶液显酸性 |
| C.NaClO4中含有离子键和共价键 |
| D.NH4ClO4只有氧化性,没有还原性 |
已知:(1)Al(OH)3电离方程式为:AlO2-+H++H2O Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-
(2)无水AlCl3晶体沸点为182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:
PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb
则下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是
| A.均为强电解质 |
| B.均为弱电解质 |
| C.均为离子化合物 |
| D.均为共价化合物 |
关于化学键的叙述正确的是
| A.离子化合物中只存在离子键 |
| B.非金属元素组成的化合物中可能存在离子键 |
| C.由不同种元素组成的多原子分子里,一定只存在极性共价键 |
| D.含金属元素的化合物中一定存在离子键 |
下列针对H3O+的说法中正确的是
| A.中心原子上的孤电子对数为2 |
| B.O原子采用sp2杂化, 空间构型为三角锥形 |
| C.离子中存在配位键 |
| D.纯水呈中性, 纯水中不存在H3O+微粒 |
一般情况下,前者无法决定后者的是
| A.原子核外电子排布——元素在周期表中的位置 |
| B.弱电解质的相对强弱——电离常数的大小 |
| C.分子间作用力的大小——分子稳定性的高低 |
| D.物质内部储存的能量——化学反应的热效应 |
有关说法中正确的是
| A.分子中键能越大,键长越长,则分子越稳定 |
| B.P4和CH4都是正四面体型结构的分子,且键角都为109°28ˊ |
| C.在化学反应中,某元素由化合态变为游离态,则该元素一定被还原 |
| D.电子层结构相同的简单离子,其半径随核电荷数增大而减小 |
在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
| A.范德华力、范德华力、范德华力 | B.范德华力、范德华力、共价键 |
| C.范德华力、共价键、共价键 | D.共价键、共价键、共价键 |
下列观点正确的是
| A.化合物电离时,生成的阴离子是氢氧根离子的是碱 |
| B.某化合物的熔融状态能导电,该化合物中一定有离子键 |
| C.某化合物的水溶液能导电,该化合物一定是电解质 |
| D.某纯净物在常温下为气体,则组成该物质的微粒一定含有共价键 |
试题篮
()