用一带静电的玻璃棒靠近A、B两种纯液体流,现象如右图所示据此分析,A、B两种液体分子的极性正确的是
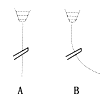
A.A是极性分子,B是非极性分子 B.A是非极性分子,B是极性分子
C.A、B都是极性分子 D.A、B都是非极性分子
下列叙述正确的是
| A.SiO2和CO2中,Si和O、C和O 之间都是共价键 |
| B.离子化合物中一定有金属元素 |
| C.蛋白质溶液、淀粉溶液和蔗糖溶液都是胶体 |
| D.共价化合物中各原子都满足8电子稳定结构 |
下列物质中,属于含有极性共价键的离子化合物的是
| A.MgCl2 | B.Br2 | C.KOH | D.CH3COOH |
下列物质中,属于含有极性共价键的离子化合物的是
| A.MgCl2 | B.Br2 | C.KOH | D.CH3COOH |
现有如下各种说法:①在水中氢、氧原子间均以化学键相结合 ②硅晶体熔化需要克服分子间作用力 ③离子键是阳离子和阴离子的相互吸引力 ④根据电离方程式HCl===H++Cl-,判断HCl分子里存在离子键⑤有化学键断裂的变化属于化学变化。上述各种说法正确的是
| A.都不正确 | B.① ② ⑤ | C.② ④ ⑤ | D.① ② ③ |
下列关于化学键的说法正确的是
①含有金属元素的化合物一定是离子化合物 ②第ⅠA族和第ⅦA族原子化合时,一定生成离子键 ③由非金属元素形成的化合物一定不是离子化合物 ④活泼金属与非金属化合时,能形成离子键
⑤含有离子键的化合物一定是离子化合物 ⑥离子化合物中可能同时含有离子键和共价键
| A.①②⑤ | B.④⑤⑥ | C.①③④ | D.②③⑤ |
常温下,1 mol化学键断裂成气态原子所需消耗的能量用E表示。结合表中信息判断下列说法不正确的是
| 共价键 |
H—H |
F—F |
H—F |
H—Cl |
H—I |
| E(kJ·mol-1) |
436 |
157 |
568 |
432 |
298 |
A.432 kJ·mol-1>E(H—Br)>298 kJ·mol-1
B.表中最稳定的共价键是H—F键
C.H2(g)―→2H(g) ΔH=+436 kJ·mol-1
D.H2(g)+F2(g)="==2HF(g)" ΔH=-25 kJ·mol-1
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同。下列叙述错误的是
| A.元素的非金属性次序为c>b>a |
| B.a和其他3种元素均能形成共价化合物 |
| C.d和其他3种元素均能形成离子化合物 |
| D.元素a 、b、c各自最高和最低化合价的代数和分别为0、4、6 |
下列说法中正确的是
| A.KOH中含有离子键也含有共价键,属于离子化合物 |
| B.HCl中存在离子键,属于离子化合物 |
| C.含有共价键的化合物一定是共价化合物 |
| D.阴、阳离子间通过静电引力而形成的化学键叫做离子键 |
试题篮
()