下列说法不正确的是 ( )
| A.σ键比π键重叠程度大,形成的共价键强 |
| B.两个原子之间形成共价键时,最多有一个σ键 |
| C.气体单质中,一定有σ键,可能有π键 |
| D.N2分子中有一个σ键,2个π键 |
下面有关离子化合物的说法正确是
| A.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物。 |
| B.离子键只存在于离子化合物中,离子化合物中一定含有离子键 |
| C.离子化合物中不可能含有共价键 |
| D.离子化合物受热融化破坏化学键,吸收能量,属于化学变化 |
下列叙述与分子间作用力无关的是 ( )
| A.气体物质加压或降温时能凝结或凝固 |
| B.干冰易升华 |
| C.氟、氯、溴、碘单质的熔沸点依次升高 |
| D.氯化钠的熔点较高 |
下列说法一定正确的是
| A.其水溶液导电的一定是离子化合物 |
| B.熔融态导电的一定是离子化合物 |
| C.固态导电的一定是金属单质 |
| D.固态不导电但熔融态导电的一定是离子化合物 |
下列化合物中所有化学键都是共价键的是
| A.Na2O2 | B.NaOH | C.BaCl2 | D.CH4 |
下列分子:①BF3,②CCl4,③NH3,④H2O,⑤CH3Cl,⑥CS2。其中只含极性键的非极性分子有( )
| A.①②⑥ | B.①②⑤ |
| C.②⑤③ | D.①②③ |
下列关于化学键的说法中正确的是
| A.构成单质分子的微粒一定含有共价键 |
| B.由非金属组成的化合物不一定是共价化合物 |
| C.非极性键只存在于双原子单质分子里 |
| D.不同元素组成的多原子分子里的化学键一定是极性键 |
下列反应过程中,同时有离子键、极性键和非极性键的断裂和形成的是
A.NH4Cl  NH3↑+HCl↑ NH3↑+HCl↑ |
B.NH3+CO2+H2O===NH4HCO3 |
| C.2Na2O2+2H2O===4NaOH+O2 ↑ | D.2NaOH+Cl2===NaCl+NaClO+H2O |
下列有关化学用语表示正确的是
A.CO2分子比例模型: |
B.S2-的结构示意图: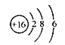 |
| C.质子数为53,中子数为78的碘原子:131 53I |
D.过氧化氢的电子式:H+ H H |
在下列变化过程中,被破坏的作用力正确的是
| A.干冰升华一一共价键 |
| B.二氧化硅熔融——范德华力 |
| C.氢氧化钠熔融——离子键、共价键 |
| D.硫酸氢钠溶于水——离子键、共价键 |
下列表达方式错误的是
A.氢有三种核素:H、D、T B.S2-的结构示意图:
C.石英中存在SiO2分子 D.CO2分子的结构式:O=C=O
试题篮
()