下列电解质溶液的有关叙述正确的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol/L NaOH标准溶液滴定HCI与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol/L),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1mol/L盐酸③0.1 mol/L氯化镁溶液④0.1 mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |
下列说法正确的是
| A.常温下,将pH=11的氨水稀释到原体积的10倍后,溶液的pH=10 |
| B.为确定某酸.H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol/L NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol/L),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1 mol/L盐酸 ③0.1 mol/L氯化镁溶液④0.1 mol/L硝酸银溶液中,则Ag+浓度:①>④=②>③ |
下列有关实验的原理、方法和结论都正确的是
| A.将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH变化大 |
| B.用CH3COOH溶液作导电性实验,灯光较暗,说明CH3COOH是弱电解质 |
| C.向滴有酚酞的Na2CO3溶液中逐滴加入Ba(NO3)2,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
有常温下物质的量浓度均为0.1 mo/L的①氨水②NH4Cl溶液③Na2CO3溶液④NaHCO3溶液,下列说法正确的是
| A.4种溶液pH的大小顺序:①>④>③>② |
| B.等体积的①和②溶液混合后pH>7,c(NH3·H2O)>c( NH4+) |
| C.溶液①、③由水电离产生的c(OH― ):①<③ |
| D.溶液③、④等体积混合后,溶液中c(CO32-)>c(HCO3) |
下列说法正确的是
| A.NaHCO3和Na2CO3混合溶液中,一定有 c(Na+)+c(H+)=c(OH-)+c(HCO3-) +c(CO32-) |
| B.浓度均为0.1 mol·L-1的下列溶液,pH由大到小排列顺序为 NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
| C.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
| D.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比为1∶2 |
对于(NH4)2SO4溶液,下列说法正确的是
A.溶液中存在电离平衡:(NH4)2SO4 2NH4+ + SO42- 2NH4+ + SO42- |
| B.向溶液中滴加少量浓硫酸,c(NH4+)与c(SO42-)均增大 |
| C.加水稀释,溶液中所有离子的浓度均减小 |
| D.溶液中:c(SO42-)=2c(NH4+) + 2c(NH3·H2O) |
25℃时,0.01 mol·L-1两种弱酸溶液的pH如表,下列说法正确的是
| A.相同pH的两种酸溶液中,CH3COOH溶液中水电离的c(H+)较大 |
| B.物质的量浓度相同的CH3COONa与NaCN 溶液中,CH3COONa溶液pH较大 |
| C.等体积pH相同的两种酸溶液,分别滴加NaOH溶液至恰好中和,消耗等量的NaOH |
| D.HCN的电离平衡常数(Ka)与CN—的水解平衡常数(K)存在如下关系:Ka•K=Kw |
下列说法正确的是
| A.中和等体积、等物质的量浓度盐酸和醋酸溶液,盐酸所需NaOH溶液多于醋酸 |
| B.常温下,20 LpH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
C.向0.1 mol/LCH3COOH溶液中加入少量CH3COONa固 体,溶液中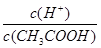 增大 增大 |
| D.一定温度下,10mL 0.50mol·L—1 NH4Cl溶液与20mL 0.25mol·L—1 NH4C1溶液含NH4+物质的量相同 |
已知:H2SO3的Ka1=1.3×10-2,Ka2=6.3×10-8;H2CO3的Ka1=4.2×10-7,Ka 2=5.6×10-11。现将标准状况下2.24L的CO2和2.24L的SO2分别通入两份150mL1mol/LNaOH溶液中,关于两溶液的比较下列说法正确的是
| A.c(HCO3-)<c(CO32-) |
| B.两溶液都能使酸性高锰酸钾溶液褪色 |
| C.c(HCO3-)>c(HSO3-) |
| D.c(CO32-)+c(HCO3-)=c(SO32-)+c(HSO3-) |
下列各溶液中,微粒的物质的量浓度关系正确的是
| A.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+) = c(NO3-) |
| B.1.0 mol·L-1Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+) |
| C.1.0 mol·L-1 NH4Cl溶液:c(NH4+) = c(Cl-) |
| D.醋酸钠溶液:c(Na+) >c(CH3COO-)>c(H+)>c(OH-) |
已知:H2SO3的Ka1=1.3×10-2,Ka2=6.3×10-8;H2CO3的Ka1=4.2×10-7,Ka2=5.6×10-11。现将标准状况下2.24L的CO2和2.24L的SO2分别通入两份150mL1mol/LNaOH溶液中,关于两溶液的比较下列说法正确的是
| A.c(HCO3-)<c(CO32-) |
| B.两溶液都能使酸性高锰酸钾溶液褪色 |
| C.c(HCO3-)>c(HSO3-) |
| D.c(CO32-)+ c(HCO3-)=c(SO32-)+ c(HSO3-) |
下列有关溶液中离子浓度的关系,不正确的是
| A.NaHCO3溶液中存在:c(OH-)=c(H2CO3)+c(H+) |
| B.常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-) |
| C.0.2 mol/LNH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+) |
| D.0.2 mol/L 的 CH3COOH 溶液中c(H+)小于0.1 mol/L 的 CH3COOH 中c(H+)的两倍 |
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表达不正确的是
| A.在NaHCO3溶液中加入与其等物质的量的NaOH ,溶液中的阴离子只有CO32-和OH- |
| B.NaHCO3溶液中:c(HCO3- ) +c(H2CO3) +c(CO32-)=c(Na+) |
| C.相同温度下,l0mL 0.lmol·L-1的醋酸与100mL 0.01 mol·L-1的醋酸中H+的物质的量不相等 |
| D.相同温度下,中和体积与pH都相同的HCI溶液和CH3COOH溶液所消耗的NaOH的物质的量,后者多 |
关于溶液的下列说法正确的是
| A.c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在 |
| B.水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 |
C.往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中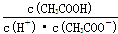 增大 增大 |
| D.等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32-)的大小关系为:②>④>③>① |
下列溶液中各微粒的浓度关系正确的是
| A.物质的量浓度相等的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2三种溶液, c (NH4+)的大小顺序为:①>②>③ |
| B.pH相等的NaF与CH3COOK溶液:c(Na+)-c(F —)>c(K+)-c(CH3COO—) |
| C.0.2 mo1·L —1的Na2CO3溶液:c(OH—)=c(HCO3—)+c(H+)+2c(H2CO3) |
| D.0.2 mo1·L —1 HCl与0.1 mo1·L —1 NaAlO2溶液等体积混合:c(Cl—)> c(Na+)>c(Al3+)>c(H+)>c(OH—) |
试题篮
()