某温度下,100g饱和氯化钠溶液中含有氯化钠26.5g。若向此溶液中添加3.5g氯化钠和6.5g水,则所得溶液的溶质质量分数是
| A.30% | B.100% |
| C.26.5% | D.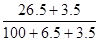 ×100% ×100% |
下列各物质溶液中,指定微粒浓度之间的关系不正确的是( )
| A.饱和NH4Cl溶液中:c(H+)+ c(NH4+)= c(Cl―)+ c(OH―) |
| B.0.1mol/LNaHCO3溶液中:c(HCO3―)+ c(CO32―)+ c(H2CO3)=0.1mol/L |
| C.饱和NaHS溶液中:c(Na+)> c(HS―)> c(H+)> c(OH―) |
| D.0.1mol/LCH3COONa溶液中:c(CH3COO―)> c(OH―) |
下列变化规律不正确的是 ( )
| A.温度升高,水的电离平衡向右移动 |
| B.加水稀释时,醋酸钠的水解平衡向左移动 |
| C.增大压强,对醋酸的电离平衡影响不大 |
| D.向氯化铁溶液中加入氧化钠,水解平衡向右移动 |
在四个不同的容器中进行合成氨的反应。根据下列在相同时间内测定的结果,判断生成氨的速率最快的是
| A.v (N2)=0.05mol·L-1·s-1 | B.v (H2)=0.3mol·L-1·min-1 |
| C.v (N2)="0.2" mol·L-1·min-1 | D.v (NH3)="0.3" mol·L-1·min-1 |
含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为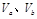 ,则两者的关系正确的是
,则两者的关系正确的是
A.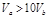 |
B.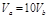 |
C.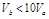 |
D.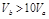 |
常温下,向20.00 mL 0.1000 mol·L—1 (NH4)2SO4溶液中逐滴加入0.2000 mol·L—1NaOH时,溶液的pH与所加NaOH溶液体积的关系如右下图所示(不考虑挥发)。下列说法正确的是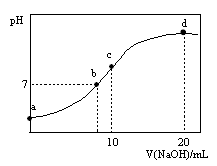
A.点a所示溶液中:c(NH )>c(SO )>c(SO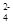 )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
B.点b所示溶液中:c(NH )=c(Na+)>c(H+)=c(OH-) )=c(Na+)>c(H+)=c(OH-) |
C.点c所示溶液中:c(SO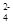 )+ c(H+)= c(NH3·H2O )+ c(OH-) )+ c(H+)= c(NH3·H2O )+ c(OH-) |
D.点d所示溶液中:c(SO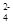 )>c(NH3·H2O )>c(OH-)>c(NH )>c(NH3·H2O )>c(OH-)>c(NH ) ) |
有100 mL 3 mol·L-1的氢氧化钠溶液和100 mL 1 mol·L-1的氯化铝溶液。按如下两种方法进行实验:
①将氢氧化钠溶液分多次加入到氯化铝溶液中;
②将氯化铝溶液分多次加入到氢氧化钠溶液中。
比较两次实验,结果是( )
| A.现象相同,最终沉淀量相等 | B.现象不同,最终沉淀量不相等 |
| C.现象相同,最终沉淀量不相等 | D.现象不同,最终沉淀量相等 |
在HNO3、Al(NO3)3和Mg(NO3)2的混合溶液中逐滴加入NaOH溶液,则消耗NaOH溶液的体积(x轴)与生成沉淀(y轴)之间的关系表示正确的是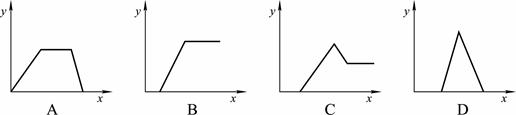
下列变化规律不正确的是 ( )
| A.温度升高,水的电离平衡向右移动 |
| B.加水稀释时,醋酸钠的水解平衡向左移动 |
| C.增大压强,对醋酸的电离平衡影响不大 |
| D.向氯化铁溶液中加入氧化钠,水解平衡向右移动 |
关于2molCO2的叙述,正确的是 (相对原子质量 C—12 O—16)
| A.质量为88g | B.摩尔质量为88g/mol |
| C.分子数为1.204×1024个 | D.常温下,体积为44.8L |
下列溶液中,Na+ 浓度最大的是( )
| A.1mol/L Na2SO4溶液200mL | B.0.9mol/L Na3PO4溶液200mL |
| C.2.5mol/L NaOH 溶液100mL | D.1mol/L NaHCO3溶液300mL |
某盐的混合物中含有0.2 mol Na+、0.4 mol Mg2+、0.4 mol Cl -,则SO42- 为( )
| A.0.1 mol | B.0.3 mol | C.0.5 mol | D.0.15 mol |
对于可逆反应M+N Q 达到限度的标志是( )
Q 达到限度的标志是( )
| A.M、N、Q三种物质的浓度一定相等 | B.M、N全部变成了Q |
| C.M、N、Q三种物质的浓度不再变化 | D.反应已经停止 |
化学知识在生活中有重要意义,下列说法不正确的是
| A.草木灰(含有K2CO3)水溶液可以用于洗涤油污 |
| B.乙醇、乙酸和甲醛广泛应用于食品加工 |
| C.捕获排放的CO2能降低地球的温室效应 |
| D.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
试题篮
()