下列溶液中,微粒的物质的量浓度关系一定正确的是( )
A.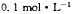 的硫化钾溶液中: 的硫化钾溶液中: |
B.常温下,pH=7的CH3COOH与CH3COONa的混合液中: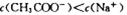 |
C.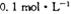 的NH4Cl溶液中: 的NH4Cl溶液中: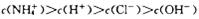 |
D.pH=3的一元酸和pH=11的一元强碱等体积混合: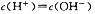 |
(10分)已知:乙二酸俗称草酸(结构简式为HOOC—COOH,可简写为H2C2O4)。
5℃时,草酸的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;
碳酸(H2CO3)的电离平衡常数为K1=4.5×10-7,K2= 4.7×10-11。
草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。
回答下列问题:
(1)写出水溶液中草酸的电离方程式 ;
(2)相同条件下等物质的量浓度的Na2C2O4溶液的pH比Na2CO3溶液的pH (填“大”、“小”或“相等”);
(3)常温下将0.4 mol/L的KOH溶液20 mL与0.2 mol/L的草酸溶液20 mL混合,则混合后溶液中阴离子浓度的大小顺序为__________________________;
(4)实验室常用酸性高锰酸钾溶液滴定草酸来测定草酸溶液的浓度。高锰酸钾溶液常用 (填“稀硫酸”、“稀硝酸”、“稀盐酸”)酸化,已知酸性高锰酸钾和草酸反应的现象是有气泡产生,紫色消失,其反应的离子方程式为 ;
(5)25℃时向20 mL碳酸钙的饱和溶液中逐滴加入8.0×10-4 mol/L的草酸钾溶液20 mL,
能否产生沉淀 (填“能”或“否”).
已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下还原法,在酸性介质中用FeSO4等将+6价铬还原成+3价铬。
具体流程如下: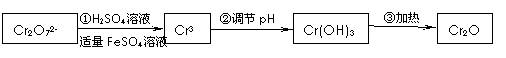
有关离子完全沉淀的pH如下表:
| 有关离子 |
Fe2+ |
Fe3+ |
Cr3+ |
| 完全沉淀为对应氢氧化物的pH |
9.0 |
3.2 |
5.6 |
(1)写出Cr2O72―与FeSO4溶液在酸性条件下反应的离子方程式 。
(2)还原+6价铬还可选用以下的 试剂(填序号)。
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
在操作②中调节pH应分2次进行,第1次应先调节溶液的pH范围约在 (填序号)最佳,第2次应调节溶液的pH范围约在 (填序号)最佳
A.3~4 B.6~8 C.10~11 D.12~14
用于调节溶液的最佳试剂为: (填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量浓度 (mol·L-1) |
NaOH物质的量浓度 (mol·L-1) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.2 |
0.1 |
pH<7 |
请回答:
(1)从第①组情况分析,HA是强酸还是弱酸 。该组所得混合溶液中由水电离出的c(OH-) = mol·L-1。
(2)第②组情况表明,c 0.2(选填“大于”、“小于”或“等于”)。该混合液中离子浓度c(A-)与c(Na+)的大小关系是 。
(3)从第③组实验结果分析,说明此时HA的电离程度 NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中各离子浓度由大到小的顺序是 。
(4)由上述所涉及的溶质组成以下四组等体积溶液:
甲:0.1mol/LNaA; 乙:0.1mol/LNaA和0.1mol/LHA;
丙:0.1mol/LHA; 丁:0.1mol/LNaA和0.1mol/LNaOH;
则A-离子浓度由大到小的顺序为 > > > 。(填写序号)
已知25 ℃时部分弱电解质的电离平衡常数数据如下表:
| 化学式 |
CH3COOH |
H2CO3 |
HClO |
|
| 平衡 常数 |
Ka=1.8×10-5 |
 = =4.3×10-7 |
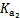 = =5.6×10-11 |
Ka= 3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1 mol·L-1的四种溶液:a.CH3COONa b.Na2CO3 c.NaClO
d.NaHCO3;pH由小到大的排列顺序是 (用字母表示)。
(2)常温下,0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 (填序号)。
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-) D.c(OH-)/c(H+)
(3)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 (填“大于”“小于”或“等于”)CH3COOH的电离平衡常数。理由是 。 
(4)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol·L-1(填精确值), = 。
= 。
下列叙述中,不正确的是
| A.0.1 mol?L-1 CH3COOH溶液加水稀释,n(H+)增大 |
| B.0.2 mol?L-1盐酸与等体积0.05 mol?L-1 Ba(OH)2溶液混合后,溶液pH为1 |
| C.向含等浓度的KCl和KI的混合溶液,滴加少量AgNO3溶液生成黄色沉淀,说明同温度下Ksp(AgCl)大于Ksp(AgI) |
| D.若NH4HCO3溶液、NH4HSO4溶液和NH4NO3溶液中c(NH4+)相等,则 |
c(NH4HSO4) < c(NH4NO3) < c(NH4HCO3)
有X、Y、Z、W四种物质的水溶液,它们分别是Na2CO3、NaOH、CH3COOH和NaCl中的一种。已知X、Y两溶液中水的电离程度相同,X、Z两溶液的pH相同,请回答下列问题:
(1)X是 ,Z是 ;
(2)Z、W两溶液中水的电离程度由大到小的顺序为 (用化学式表示);
(3)写出Z溶液与过量Y溶液反应的离子方程式 ;
(4)X、Y两溶液恰好完全反应后,溶液中各离子浓度由大到小的顺序是
。
有常温下物质的量浓度均为0.1 mo/L的①氨水②NH4Cl溶液③Na2CO3溶液④NaHCO3溶液,下列说法正确的是
| A.4种溶液pH的大小顺序:①>④>③>② |
| B.等体积的①和②溶液混合后pH>7,c(NH3·H2O)>c( NH4+) |
| C.溶液①、③由水电离产生的c(OH― ):①<③ |
| D.溶液③、④等体积混合后,溶液中c(CO32-)>c(HCO3) |
下列溶液中微粒浓度关系一定正确的是
| A.室温时,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B.室温时,pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) |
| C.0.1 mol·L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) |
| D.0.1 mol·L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
某酸性溶液中只含NH4+、C1-、H+、OH-四种离子,下列说法正确的是
| A.溶液中离子浓度可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-) |
| B.该溶液不能由等物质的量浓度、等体积的盐酸和氨水混合而成 |
| C.可由pH=3的盐酸与pH=11的氨水等体积混合而成 |
| D.再通入适量氨气,溶液中离子浓度可能为:c(NH4+)>c(C1-)>c(H+)>c(OH-) |
工业上常用还原沉淀法处理含铬废水(Cr2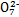 和Cr
和Cr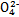 ),其流为:
),其流为:
Cr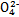
 Cr2
Cr2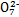
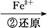 Cr3+
Cr3+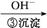 Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr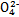 (黄色)+2H+
(黄色)+2H+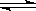 Cr2
Cr2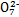 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) 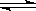 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在
下列有关说法中正确的是
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr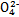 浓度增大 浓度增大 |
B.步骤①中当2v(Cr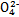 )=v(Cr2 )=v(Cr2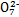 )时,说明反应2Cr )时,说明反应2Cr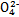 (黄色)+2H+ (黄色)+2H+ Cr2 Cr2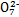 (橙色)+H2O达到平衡状态 (橙色)+H2O达到平衡状态 |
C.步骤②中,若要还原1 mol Cr2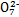 ,需要12 mol (NH4)2Fe(SO4)2·6H2O ,需要12 mol (NH4)2Fe(SO4)2·6H2O |
| D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽 |
常温下,关于下列溶液的叙述错误的是
| A.CH3COOH分子可以存在于pH=8的碱性溶液中 |
| B.1mol/L氨水与0.5mol/L氨水中c(OH-)之比是2:1 |
| C.甲酸溶液和一定量NaOH溶液恰好完全反应,溶液中c(HCOO-)<c(Na+) |
| D.等体积等pH的醋酸和盐酸分别加水稀释至a mL和b mL,稀释后溶液pH均为5,则a>b |
25℃时,0.01 mol·L-1两种弱酸溶液的pH如表,下列说法正确的是
| A.相同pH的两种酸溶液中,CH3COOH溶液中水电离的c(H+)较大 |
| B.物质的量浓度相同的CH3COONa与NaCN 溶液中,CH3COONa溶液pH较大 |
| C.等体积pH相同的两种酸溶液,分别滴加NaOH溶液至恰好中和,消耗等量的NaOH |
| D.HCN的电离平衡常数(Ka)与CN—的水解平衡常数(K)存在如下关系:Ka•K=Kw |
下列各溶液中,微粒的物质的量浓度关系正确的是
| A.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+) = c(NO3-) |
| B.1.0 mol·L-1Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+) |
| C.1.0 mol·L-1 NH4Cl溶液:c(NH4+) = c(Cl-) |
| D.醋酸钠溶液:c(Na+) >c(CH3COO-)>c(H+)>c(OH-) |
已知:H2SO3的Ka1=1.3×10-2,Ka2=6.3×10-8;H2CO3的Ka1=4.2×10-7,Ka2=5.6×10-11。现将标准状况下2.24L的CO2和2.24L的SO2分别通入两份150mL1mol/LNaOH溶液中,关于两溶液的比较下列说法正确的是
| A.c(HCO3-)<c(CO32-) |
| B.两溶液都能使酸性高锰酸钾溶液褪色 |
| C.c(HCO3-)>c(HSO3-) |
| D.c(CO32-)+ c(HCO3-)=c(SO32-)+ c(HSO3-) |
试题篮
()