在一体积固定的密闭容器中加入反应物A、B,发生反应:A(g)+2B(g)=3C(g)。反应2 min后,A的浓度从开始时的1.0 mol·L-1降到0.8 mol·L-1。已知反应开始时B的浓度是1.2 mol·L-1。求:(1)2 min末B、C的浓度。(2)以单位时间内A的浓度的减小来表示2 min内该反应的平均速率。
在一密闭的2L容器里装有4 mol SO2和2 mol O2,在一定条件下开始反应生成SO3。2 min末测得容器中有3.6 mol SO2,试计算:
(1)2 min末SO3的浓度
(2)2 min内SO2的平均反应速率
(3)O2的转化率
将N2和H2按一定比例混合,其密度是相同状况下H2的3.6倍,取出0.5 mol该混合气体充入密闭容器里,使之发生反应并在一定条件下达到平衡,已知反应达平衡后容器内压强是相同条件下反应前的0.76倍,试求:
(1)反应前混合气体中N2和H2的体积比。
(2)达平衡时混合气体中氨的物质的量。
(3)平衡时N2的转化率。
(4分)在合成氨时,将1体积氮气和3体积氢气混合后通过合成塔中的催化剂,若从塔中导出的混合气体中,氨气的体积分数为12%,求N2和H2的体积分数各为多少?
将6 mol H2和3 mol CO充入容积为1 L的密闭容器中,进行如下反应:2 H2(气) + CO(气) 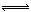 CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气)
CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气) 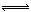 2 H2(气) + CO(气)的平衡常数K
2 H2(气) + CO(气)的平衡常数K
将A、B以物质的量之比为3:1的比例混合于2L的密闭容器中,发生如下反应:2A(g)+B(g)  xC(g)+D(g),经4min后,测得D的浓度为
xC(g)+D(g),经4min后,测得D的浓度为 ,A、B物质的量浓度之比为5:1,C的平均反应速率是
,A、B物质的量浓度之比为5:1,C的平均反应速率是 。
。
求:(1)B的转化率是多少?
(2)这4min内 A的平均反应速率是多少。
(3)x值是多少?
在常压和500℃时把O2和SO2按 1:2 体积比混合,如果混合前O2有 10 mol,平衡时SO3占总体积的91% ,求:(1)平衡时有多少摩O2转化? (2)混合气中SO2的体积分数(3)SO2的转化率
在500℃容积为2升的密闭容器中充入SO2和O2,其中SO2的浓度为1mol/L,经10秒后,达到平衡,2SO2(g)+O2(g) 2SO3(g),此时容器中SO3的浓度为0.9mol/L,O2的物质的量为2.1mol,试求:① SO2的转化率;② O2的起始浓度(mol/L);③ SO2的平均反应速率(mol/L· min)
2SO3(g),此时容器中SO3的浓度为0.9mol/L,O2的物质的量为2.1mol,试求:① SO2的转化率;② O2的起始浓度(mol/L);③ SO2的平均反应速率(mol/L· min)
把 3mol A 和 2.5mol B 混合于 2L 的密闭容器中,使它们发生反应:
3A(气) + B(气)  xC(气) + 2D(气)
xC(气) + 2D(气)
经5min后达到平衡生成1mol D,并测定C的平均速率为0.1 mol/L·min,则此反应中的B的转化率为________,C的系数为_______________,A的平衡浓度为_____________。
20%,2, 0.75 mol /L
在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)NO的平衡浓度c(NO)= 。
(2)用O2表示从0~2s内该反应的平均反应速率v= 。
(3)下图中表示NO2变化的曲线是 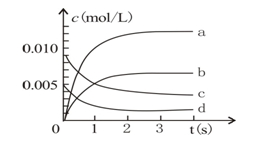
(4)800℃时,容器内起始压强和平衡后压强之比为___________________
(共10分)已知合成氨反应为:N2 + 3H2 2NH3,在一定温度下,向2L密闭容器中,加入2molN2和5molH2,一定条件下使之反应,经过2min后达到平衡状态并测得NH3为0.4mol,求:
2NH3,在一定温度下,向2L密闭容器中,加入2molN2和5molH2,一定条件下使之反应,经过2min后达到平衡状态并测得NH3为0.4mol,求:
(1)以N2表示这2min内该反应的反应速率?
(2)此时氢气的转化率?
(3)平衡时NH3的体积分数?(保留1位小数)
(4)平衡时容器中的压强与开始压强之比?
(5)平衡时容器中气体的平均摩尔质量?
某反应,在不同反应时间各物质的量变化情况如图所示。则该反应的反应物(用A、B、C的字母填写)化学方程式为 ;
若反应在5L的密闭容器中进行,反应进行到2min时用A表示的化学反应速率为 。2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了 状态。
在一定温度下,将0.20 mol 的四氧化二氮气体充入1L的固定的密闭容器中,每隔一段时间对该容器内的物质进行一次分析,得到如下数据:
 时间 (s)浓度 mol·L-1 |
0 |
20 |
40 |
60 |
80 |
100 |
| C(N2O4) |
0.20 |
C1 |
0.10 |
C3 |
C4 |
C5 |
| C(NO2) |
0.00 |
0.12 |
C2 |
0.22 |
0.22 |
0.22 |
根据表格提供数据,请回答下列各小题:
⑴该反应的化学方程式为:
表示C2 C3 C4 (填 < , > 或 = )
⑵ 20S时,四氧化二氮的浓度C1=
在0~20 S内四氧化二氮的平均反应速度为
在容积为5L的密闭容器中,通入5 mol N2和8 mol H2,在一定条件下反应生成NH3,当反应进行到2 min时,测得容器内有4 mol NH3。则:
 (1)2 min时,容器内n(N2)== ,c(H2)== 。
(1)2 min时,容器内n(N2)== ,c(H2)== 。
(2)2 min内,以N2表示的平均反应速率v(N2)== 。
 (3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为:
(3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为:
试题篮
()