把2.5 mol A和2.5 mol B混合盛入2 L容积的密闭容器里发生反应3A(g)+B(g) x C(g)+ 2D(g),经5s后反应达平衡。在此5s内C的平均反应速率为0.2 mol·L-1·s-1,同时生成1 mol D。试求:
x C(g)+ 2D(g),经5s后反应达平衡。在此5s内C的平均反应速率为0.2 mol·L-1·s-1,同时生成1 mol D。试求:
(1)试算x的值;
(2)达平衡时B的转化率;
(3)若达平衡时,该反应放出Q kJ的热量,写出该反应的热化学方程式;
(4)若温度和压强维持不变,达平衡时容器内气体的体积是多少?
某温度下,在一固定容积的密闭容器中投入一定物质的量的N2与H2进行可逆反应:N2(g)+3H2(g)  2NH3(g);在2 min时达到平衡状态,此时c(N2)=5.00 mol·L-1,c(H2)=10.00 mol·L-1,c(NH3)=5.00 mol·L-1。
2NH3(g);在2 min时达到平衡状态,此时c(N2)=5.00 mol·L-1,c(H2)=10.00 mol·L-1,c(NH3)=5.00 mol·L-1。
试求:(1)该温度下反应的平衡常数
(2)H2的起始浓度
(3)用N2表示该反应的平均反应速率
(4)N2的转化率
要使0.1 mol/L的醋酸溶液中c(H+)/c(CH3COOH)值、pH均增大,可采取的措施是 ( )
A 加水 B 升高温度 C 加少量冰醋酸 D 加少量CH3COONa固体
(6分)将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡: 2SO2 + O2 2SO3 测得平衡时混合物总的物质的量为5mol,求:
2SO2 + O2 2SO3 测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率。
( 8分)将物质的量均为3.00mol物质A、B混合于5L容器中,发生如下反应 3A+B 2C,在反应过程中C的物质的量分数随温度变化如图所示:
2C,在反应过程中C的物质的量分数随温度变化如图所示:
T0对应的反应速率V正和V逆的关系是_____(用含“>”“<”“=”表示,下同);
(2) 此反应的正反应为______热反应;
(3) X、Y两点A物质正反应速率的大小关系是______________;
(4) 温度T<T0时,C%逐渐增大的原因是________________________;
(5) 若Y点的C的物质的量分数为25%,则参加反应的A的物质的量为_______;若Y点时所耗时间为2min,则B物质的反应速率为__________。
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的
曲线如右图所示,下列描述正确的是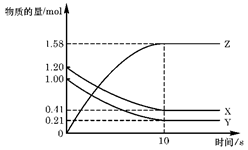
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s) |
| B.反应开始时10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始时10s,Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+Y(g) Z(g) Z(g) |
反应4A(s)+3B(g)===2C(g)+D(g),经2min后,B的浓度减少了0.6mol/L。下列反应速率的表示正确的是( )
A.用A表示的反应速率是0.4mol/(L•min)
B.分别用B、C、D表示的反应速率其比值是3:2:1
C .2min末时
.2min末时 的反应速率,用B表示是0.3mol/(L•min)
的反应速率,用B表示是0.3mol/(L•min)
D. υB=0.3mol/(L•min)和υC=0.2mol/(L•min),都表示该反应在这一时间内的反应速率
 当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 。
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 。
⑷在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀。制备CuCl的离子方程式是 。
28.(9分)下列一句话中叙述了两个值,前者记为M,后者记为N,M和N的关系从A、B、C、D中选择
A. M>N B. M<N C. M="N" D. 无法比较
⑴相同温度下,1L 1mol/L 的NH4Cl溶液中的NH4+个数和2 L 0.5mol·L-1NH4Cl溶液中NH4+的个数: ;
⑵相同温度下,pH值为12的烧碱溶液中水的电离度和pH值为12的CH3COONa溶液中水的电离度: ;
⑶两份室温时的饱和石灰水,一份升温到50℃;另一份加入少量CaO,恢复至室温,两溶液中的c(Ca2+): ;
⑷常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中c(HCO3-): ;
⑸将pH值为2的醋酸和盐酸都稀释相同倍数所得稀溶液的pH值: ;
⑹常温下0.1mol/L的CH3COOH与0.1mol/LCH3COONa等体积混合后溶液中c(Na+)和c(CH3COO-): ;
⑺同 温度下,0.1mol/LFeCl3溶液中Fe3+水解百分率与0.01mol·L-1FeCl3溶液中Fe3+的水解百分率: ;
温度下,0.1mol/LFeCl3溶液中Fe3+水解百分率与0.01mol·L-1FeCl3溶液中Fe3+的水解百分率: ;
⑻室温下某强酸和某强碱溶液等体积混合后,溶液的pH值为7, 原酸溶液和原碱溶液的物质的量浓度: ;
原酸溶液和原碱溶液的物质的量浓度: ;
⑼PH值相同的醋酸和盐酸,分别用蒸馏水稀释至原来的M倍和N倍,稀释后两溶液的PH值仍然相同,则M和N的关系是: 。
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒 气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、100 kPa下,ΔH=-113 kJ/mol,ΔS=-145 J/(mol·K).
气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、100 kPa下,ΔH=-113 kJ/mol,ΔS=-145 J/(mol·K).
(1)为了提高该反应的速率和NO的转化率,采取的正确措施为________.
| A.加催化剂同时升高温度 |
B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 |
| D.降低温度同时增大压强 |
(2)该反应达到平衡时若增大压强,则混合气体的 平均相对分子质量________,若升高温度,则该反应的平衡常数________(均填“增大”、“减小”或“不变”).
平均相对分子质量________,若升高温度,则该反应的平衡常数________(均填“增大”、“减小”或“不变”).
(3)在如图中画出在某时刻条件改变后的图象(其他条件不变).t1:增大NO的浓度 t2:降低温度
(4)判断该条件下反应能否自发.
在一定温度下(已知在该温度下,容器内所有物质均为气态),10 L密闭容器中加入5 mol SO2.4 mol O2,经10 min后反应达平衡时有2 mol SO2发生了反应。试计算:
(1)用SO2表示该反应的反应速率;
(2)O2的转化率;
(3)该温度下的平衡常数K(保留三位有效数字)。
下列措施对增大化学反应速率无明显效果的是
A. 分解制氧气时,加入催化剂且加热 分解制氧气时,加入催化剂且加热 |
| B.做铝与稀盐酸反应的实验时,将铝片改为铝粉 |
| C.铁与稀硫酸反应制取氢气时,改用质量分数为98%的浓硫酸 |
| D.锌与稀硫酸反应时,加入少量铜粉 |
下列关于化学反应速率的说法中正确的是
| A.根据化学反应速率的大小可以知道化学反应进行的快慢 |
B.化学反应速率为 ,是指1s时,物质的量深度为 ,是指1s时,物质的量深度为 |
| C.对任何化学反应来说,反应速率越大化学现象越明显 |
| D.化学反应速率是指一定时间内,任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
在镁与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6 mol/L,则10s内生成氢气的平均反应速率是
反应4NH3(g) + 5O2(g) 4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则表示此反应的速率正确的是( )
4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则表示此反应的速率正确的是( )
| A.v (O2) = 0.01mol·(L·s) –1 | B.v (NO) =" 0.008mol·(L·s)" –1 |
| C.v (H2O) =" 0.003mol·(L·s)" –1 | D.v (NH3) =" 0.02mol·(L·s)" –1 |
CO和H2在一定条件下可以合成乙醇:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1∶2的物质的量之比反应生成乙醇 |
| D.反应体系中乙醇的物质的量浓度不再变化 |
试题篮
()