已知反应:PC15(g)  PC13 (g)+ C12(g),将1.0 mol PC15充入容积为2 L的密闭容器中,一段时间后,测得PC15的浓度为0.3 mol/L,在这段时间内的平均反应速率υ(PC15)=0.4 mol/(L·min),则这段时间为
PC13 (g)+ C12(g),将1.0 mol PC15充入容积为2 L的密闭容器中,一段时间后,测得PC15的浓度为0.3 mol/L,在这段时间内的平均反应速率υ(PC15)=0.4 mol/(L·min),则这段时间为
| A.50 s | B.30 s | C.5 s | D.1 s |
四位同学在学习“化学反应速率和化学平衡”后,联系工业生产实际所发表的观点,你认为不正确的是
| A.化学反应速率理论是研究怎样在一定时间内快出产品 |
| B.化学平衡理论是研究怎样使用有限原料多出产品 |
| C.化学反应速率理论是研究怎样提高原料转化率 |
| D.化学平衡理论是研究怎样使原料尽可能多地转化为产品 |
下列说法正确的是
| A.有气体参加的化学反应,若增大压强,可增加活化分子的百分数,从而使反应速率增大 |
| B.增大反应物浓度,可增大活化分子的百分数,从而使单位时间内有效碰撞次数增多 |
| C.在化学反应中,加入催化剂只能增大正反应速率 |
| D.升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 |
对于反应4CO(g)+2NO2(g)  N2(g)+4CO2(g),以下化学反应速率的表示中,所表示反应速率最快的是
N2(g)+4CO2(g),以下化学反应速率的表示中,所表示反应速率最快的是
| A.v(CO)=1.6 mol·(L·min) -1 | B.v(NO2)=0.9 mol·(L·min) -1 |
| C.v(N2)=0.25mol·(L·min) -1 | D.v(CO2)=1.2 mol·(L·min) -1 |
一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是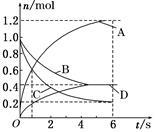
A.该反应的化学方程式为3B+4D 6A+2C 6A+2C |
B.反应进行到1 s时,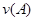 = =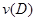 |
| C.反应进行到6s时,B的平均反应速率为0.05 mol/(L·s) |
| D.反应进行到6s时,各物质的反应速率相等 |
对于A2+3B2 = 2C+D的反应来说,以下化学反应速率的表示中,反应速率最快的是
A. (A2)=0.4 mol·L-1·s-1 B.
(A2)=0.4 mol·L-1·s-1 B. (B2)=0.8 mol·L-1·s-1
(B2)=0.8 mol·L-1·s-1
C. (C)=0.6 mol·L-1·s-1 D.
(C)=0.6 mol·L-1·s-1 D. (D)=0.6 mol·L-1·min-1
(D)=0.6 mol·L-1·min-1
在2A+B 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A、υ(A)= 0.5 mol/(L·s) B、υ(D)= 1 mol/(L·s)
C、υ(C)= 0.8 mol/(L·s) D、υ(B)= 0.3 mol/(L·s)
在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示。请认真观察下图,然后回答问题。

(1)图中反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”或“不需要”)环境先提供能量,该反应的△H= (用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+1/2O2(g) =H2O(g) △H= -241.8kJ•mol-1,该反应的活化能为167.2 kJ•mol-1,则其逆反应的活化能为 。
(3)对于同一反应,图中虚线(Ⅱ)与实线(I)相比,活化能 ,单位体积内活化分子的百分数 ,因此反应速率 ,(前面的三个空填“增大”“减小”“不变”)你认为最可能的原因是 。
用3g块状大理石与30mL3mol/L盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是: ①再加入30mL3mol/L盐酸;②改用30mL6mol/L盐酸;③改用3g粉末状大理石;④适当升高温度
| A.①②④ | B.②③④ | C.①③④ | D.①②③ |
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示,下列结论不正确的是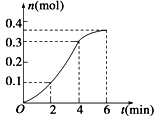
| A.反应开始2 min内平均反应速率最大 |
| B.反应速率先增大后减小 |
| C.反应2 min到第4 min内温度对反应速率的影响比浓度大 |
| D.反应在第2 min到第4 min内生成CO2的平均反应速率为前2 min的2倍 |
反应:3A(g)+B(g)=2C(g)+2D(g),在不同条件下的反应速率分别为:
①v(A)="0.6mol" /(L·min) ②v(B)=0.45mol/(L·min)
③v(C)="0.4mol" /(L·min) ④v(D)="0.45mol" /(L·min)。
则此反应在不同条件下,进行得最快的是
A.② B.①和③ C.②和④ D.①
2A(g)+B(g)  3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
A.V(A) = 0.7mol·L-1·min-1
B.V(B) = 0.3mol·L-1·min-1
C.V(C) = 0.9mol·L-1·min-1
D.V(D) = 1.1mol·L-1·min-1
在密闭容器中发生可逆反应4NH3+5O2 4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
| A.v(O2)="0.01" mol•L-1•s-1 | B.v(NH3)="0.02" mol•L-1•s-1 |
| C.v(H2O)="0.04" mol•L-1•s-1 | D.v(NO)="0.03" mol•L-1•s-1 |
在N2+3H2 2NH3的反应中,经一段时间后,NH3的物质的量浓度增加了0.6mol•L-1,在此时间内用H2物质的量浓度表示的平均速率为0.45mol/(L•s),则反应所经过的时间为
2NH3的反应中,经一段时间后,NH3的物质的量浓度增加了0.6mol•L-1,在此时间内用H2物质的量浓度表示的平均速率为0.45mol/(L•s),则反应所经过的时间为
| A.0.2s | B.1.0s | C.1.5s | D.2.0s |
试题篮
()