现有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3、Na2SO4现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀产生:
②向①的悬浊液中加入过量稀盐酸,白色沉淀部分溶解,并有气泡放出:
③取少量②的上层清液滴入硝酸银溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题:
(1)判断原白色粉末中肯定含有, ,可能含有 。
(2)写出上述实验中一定发生的有关反应的离子反应方程式: 。
过氧化氢H2O2,(氧的化合价为-1价),水溶液俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~F涉及H2O2的反应,回答相关问题:
| A.Na2O2 +2HCl=2NaCl+H2O2 |
| B.2H2O2=2H2O+O2↑ |
| C.Ag2O+H2O2=2Ag+O2↑+ H2O |
| D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O |
E.H2O2+MnSO4=MnO2 + H2SO4 F.H2O2 +2 Fe2+ +2H+=2Fe3+ +2H2O
(1)上述反应属于氧化还原反应的是(填代号)_____________。
(2)H2O2仅体现氧化性的反应是(填代号) 。
(3)H2O2仅体现还原性的反应是(填代号) 。
(4)上述反应说明H2O2、Ag2O、MnO2氧化性由强到弱的顺序是: 。
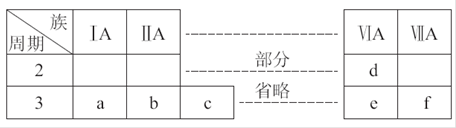
(1)画出b元素的原子结构示意图 ,并写出元素b的单质在二氧化碳中燃烧的化学方程式: 。
(2)将a、b、c三种元素的最高价氧化物对应的水化物碱性由强到弱排序: (填写物质化学式)。
(3)写出元素c的氧化物与元素a的最高价氧化物对应的水化物反应的离子方程式: 。
(4)将e、f的最高价氧化物对应的水化物酸性较强的是: (填写物质化学式)。
(5)写出d元素的氢化物(一个分子共有三个原子)电子式: ,写出f元素与该氢化物反应的离子方程式: 。
(1)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为____________________。
(2)已知: 2Fe(s)+O2(g)=2FeO(s) ΔH=-544.0kJ·mol-1
4Al(s)+3O2(g)=2Al2O3(s) ΔH=-3351.4kJ·mol-1
则Al和FeO发生铝热反应的热化学方程式为:_______________________。
按要求填空:
(1)除去下列物质中所混有的少量杂质,写出有关的反应方程式。
①Fe2O3中混有少量SiO2 ;
② NO中混有NO2 。
(2)为什么不能用加热NH4Cl固体的方式制取氨气(用化学方程式表示): 。
(3)将1.92g Cu投入到100mL某浓度的硝酸溶液中,观察到产生红棕色气体,随着反应的进行,气体颜色逐渐变浅。铜完全反应完后,共收集到1.12L气体(标准状况下测定),则此时参与反应且未被还原的硝酸物质的量为 ;所产生的气体中NO2的体积分数为 。
进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”。引发雾霾天气的污染物中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气。
I、已知反应N2O4(g) 2NO2(g) △H,随温度升高,混合气体的颜色变深。将一定量N2O4气体充入绝热容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间变化情况。下列说法能说明透光率不再发生改变的有 。
2NO2(g) △H,随温度升高,混合气体的颜色变深。将一定量N2O4气体充入绝热容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间变化情况。下列说法能说明透光率不再发生改变的有 。
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变
II、用NH3催化还原NOx可以消除氮氧化物的污染。下图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),反应原理为:

NO(g)+NO2(g)+2NH3(g) 2N2(g)+3H2O(g)。
2N2(g)+3H2O(g)。
(1)该反应的△S_________0(填“>”、“=”或“<”)。
(2)以下说法正确的是____________。
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
III、用CH4催化还原NOx也可以消除氮氧化物的污染。
(3)已知:CH4(g)的标准燃烧热为-890kJ/mol,蒸发1mol H2O(l)需要吸收44kJ热量。
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=﹣1114 kJ/mol
2NO(g)+O2(g)=2NO2(g) △H=﹣114 kJ/mol
写出CH4催化还原NO2(g)生成N2和H2O(g)的热化学方程式:_____________________。
(4)在温度为T1℃和T2℃时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
| 时间/min 温度/℃ |
0 |
10 |
20 |
40 |
50 |
| T1 |
1.2 |
0.9 |
0.7 |
0.4 |
0.4 |
| T2 |
1.2 |
0.8 |
0.56 |
… |
0.5 |
①温度为T1℃时,0~20min内,v(CH4)=___________。
②T1__________T2(填“>”或“<”,下空同);判断理由是_________________。
③T1℃时,反应CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)平衡常数K=__________。
N2(g)+CO2(g)+2H2O(g)平衡常数K=__________。
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将_______(填“增大”、“减小”或“不变”)。
把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得的浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:

(1)混合物中NaOH的质量是 g,AlCl3的质量是 g。
(2)P点所表示盐酸加入体积为 mL。
以下是由乙烯合成乙酸乙酯的几种可能的合成路线:

(1)乙酸乙酯的结构简式为 ;
(2)乙醇中含氧官能团的名称是 ;
(3)请写出反应④的化学方程式: ;
(4)写出上述几种路线中涉及到的有机化学反应基本类型:反应①: ,反应③:____________,反应⑤: 。
运用所学知识,回答下列问题。
(1)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_________________,工艺师常用______________(填物质名称)来雕刻玻璃。
(2)向硫酸铜溶液中逐滴加入KI溶液至恰好反应完全,观察到产生白色沉淀CuI,蓝色溶液变为棕色。该反应的离子方程式为 ;取一定量上述反应后的上层棕色清液于一支试管中,加入一定量的苯,振荡,此时观察到的现象是____________________________。
(3)电子工业常用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,工程师欲从制造印刷电路板的工业废水中回收铜,并获得FeCl3溶液,设计如下方案:

①滤渣的成分为 。(填化学式)
②加过量B发生反应的离子方程式为 。
③通入C发生反应的化学方程式为 。
现有下列十种物质:①液态氯化氢②小苏打 ③固体纯碱 ④二氧化碳⑤葡萄糖 ⑥氢氧化钾 ⑦氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩硫酸铁溶液
(1)上述十种物质中,属于电解质的有 ,属于非电解质的有 。
(2)有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为 。
(3)除去③中少量②的操作是 ,化学方程式为 。
(4)标准状况下,___________L ④中含有0.4mol 氧原子。
(5)现有100 mL⑩溶液中含Fe3+ 5.6g,则溶液中SO42-的物质的量浓度是 。
(6)若在⑦中缓慢加入⑥,产生的现象是 。
(7)将①加入到⑧中,⑧的导电能力变化为__________(填“增强”、“减弱”或“基本不变”)。
氯碱工业生产中用氨气检查氯气管道是否泄漏,氨气遇到氯气会产生白烟,
(1)反应还生成了一种无毒的气态单质,写出反应的化学方程式 ________________________。
(2)在该反应中,氧化剂是____________,还原产物是____________,当有1.7g的氨气参与反应时,转移的电子数目为____________。
(3)列式计算当有112 mL的氯气(已折算到标准状况)参加反应时生成白烟的质量为________ g。
按要求填空:
(1)含有相同氧原子数的CO2和CO:物质的量之比为___________;质量之比为______________。
(2)写出除去FeCl3溶液中的FeCl2所需的试剂:_______________(填化学式)
(3)海水的溴以Br-的形式存在,海水中提溴的方法通常是:向苦卤中通入Cl2是为了提取Br2,为
大量富集Br2,常先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收,该反应的离子方程式是 。
钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式: 。
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3•xH2O),写出铁发生电化学腐蚀时正极的电极反应: 。
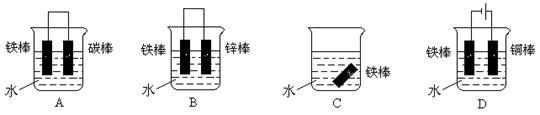
(3)下列哪个装置可防止铁棒被腐蚀 (填字母)。

(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如右图,请回答:
① B电极对应的金属是 (写元素名称),A电极的电极反应式是 。
② 若电镀前两电极的质量相同,电镀完成后, 若电镀时电路中通过的电子为0.2mol,将它们取出洗净、烘干、称量,则A、B两极质量相差 g。
用石墨电极电解500 mL含一种溶质的某蓝色溶液,如右图所示,观察到A极表面有红色固体物质生成,B极上有无色气体生成;当溶液中的原有溶质完全电解后,取出A极,洗涤、干燥、称量,电极增重1.6 g,回答下列问题:
(1)B电极发生反应的电极反应式_______________________。
(2)写出电解时反应的离子方程式______________________________。
(3)电解后溶液中H+物质的量浓度为________________,要使电解后溶液恢复到电解前的状态,则需加入____________,其质量为________________。(假设电解前后溶液的体积不变)
(4)原溶液可能是________________溶液。
(1)已知:①C3H8(g)+5O2(g)==3CO2(g)+4H2O(l) ΔH="-2220.0" kJ·mol-1
②H2O(l)==H2O(g) ΔH="+44.0" kJ·mol-1
写出丙烷燃烧生成CO2和气态水的热化学方程式:______________________。
(2)航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。我国发射的“神舟五号”载人飞船是采用先进的甲烷电池为电能来源,该电池以KOH溶液为电解质。试回答:
①负极上的电极反应为________________________________;
②消耗标准状况下的5.6 L O2时,有________mol电子发生转移。
③开始放电时,正极附近溶液的pH________(填“增大”“减小”或“不变”)。
试题篮
()