A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 |
Ag+、Na+ |
| 阴离子 |
NO3—、SO42—、Cl- |
下图Ⅰ所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27 g。常温下各烧杯中溶液的pH与电解时间t的关系如下图Ⅱ所示。据此回答下列问题: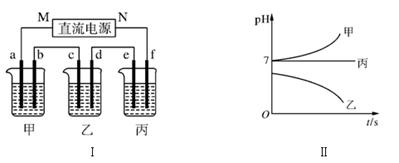
(1)M为电源的________(填“正”或“负”)极,A是________(填写化学式)。
(2)计算电极f上生成的气体在标准状况下的体积:________。
(3)写出乙烧杯的电解池反应:________________________________________________。
(4)要使丙恢复到原来的状态,应加入________ g ________(填写化学式)。
在Na+浓度为0.5mol/L的某澄清溶液中,还可能含有下表中的若干种离子:
| 阳离子 |
K+、Ag+、Mg2+、Ba2+ |
| 阴离子 |
NO3-、CO32-、SiO32-、SO42- |
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
| 序号 |
实验内容 |
实验结果 |
| Ⅰ |
向该溶液中加入足量稀HCl |
产生白色沉淀并放出0.56L气体 |
| Ⅱ |
将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 |
固体质量为2.4g |
| Ⅲ |
在Ⅱ的滤液中滴加BaC12溶液 |
无明显现象 |
试回答下列问题:
(1)实验I能确定一定不存在的阳离子是 。
(2)实验I中生成沉淀的离子方程式为 。
(3)通过实验I、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
| 阴离子 |
NO3- |
CO32- |
SiO32- |
SO42- |
| c/mol·L-1 |
|
|
|
|
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由 。
(每个方程式2分,其余每空1分,共8分)现有下列物质:
①KI ②铜 ③稀硝酸 ④NH3 ⑤NaHSO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
(1)按物质的分类方法填写表格的空白处(填物质编号)
| 分类标准 |
电解质 |
盐 |
非电解质 |
混合物 |
| 属于该类的物质 |
|
|
|
|
(2)上述某两种物质在溶液中可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式 。
(3)物质①的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为 。
某化学研究性学习小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O。已知某化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。
部分阳离子以氢氧化物形式完全沉淀时的pH如下:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Ni(OH)2 |
| pH |
5.2 |
3.2 |
9.7 |
9.2 |
回答下列问题:
(1)操作a、c中需使用的仪器除铁架台(带铁圈)、酒精灯、烧杯、蒸发皿外还需要的主要仪器为 。
(2)“碱浸”过程中发生的离子方程式是 。
(3)“酸浸”时所加入的酸是 (填化学式)。酸浸后,经操作a分离出固体①后,溶液中可能含有的金属离子是 。
(4)操作b为调节溶液的pH,你认为pH的最佳调控范围是: 。
(5)“调pH为2~3”的目的是 。
(6)产品晶体中有时会混有少量绿矾(FeSO4·7H2O),其原因可能是 __。
有一瓶澄清溶液,其中可能含有
中的几种。取该溶液进行以下实验:
(1)用pH试纸检验,表明溶液呈强酸性。排除 存在。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡,CCl4层呈紫红色。排除______存在。
(3)另取部分溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,均无沉淀产生。则可排除 存在。取部分碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
(4)另取部分上述碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
证明 存在,又排除 存在。
(5)根据上述实验事实确定:
①该溶液中肯定存在的离子是 ;
②肯定不存在的离子是 ;
③还不能确定是否存在的离子是 。
如图是广州亚运会开幕式“红棉花开迎宾来”焰火盛宴的一个场景,
请回答下列问题:
(1)焰火利用了部分金属的元素特征的 反应,该反应属于 (填“物理”或“化学”)变化。
(2)现在有一种火焰的引发是当浓H2SO4滴下去跟氯酸钾起作用时,便生成了奇臭的二氧化氯气体,且发现只有氯元素的化合价发生变化。请写出该反应的方程式 。
(3)如图所示的五元环代表A、B、C、D、E五种化合物,
圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素组成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
①D的化学式是_________.
②A、B、E中均含有的一种元素名称为______________。
③B的电子式是______________。
④C与纯碱反应的化学方程式为 。
(8分)已知在25 ℃时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数分别为
醋酸 K=1.75×10-5 次氯酸 K=2.95×10-8
碳酸K1=4.30×10-7 K2=5.61×10-11 亚硫酸 K1=1.54×10-2 K2=1.02×10-7
(1)写出碳酸的第一级电离平衡常数表达式K1=__________。
(2)在相同条件下,等浓度的CH3COONa、NaClO、Na2CO3和Na2SO3溶液中碱性最强的是________。等浓度的Na2CO3和NaHCO3的混合溶液中各离子浓度大小顺序为 。
(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列量会变小的是________。
a.c(CH3COO-) b.c(H+) c.醋酸的电离平衡常数
(4)下列离子方程式中错误的是________。
a.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-===HCO3—+HClO
b.少量SO2通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
c.过量CO2通入澄清石灰水中:CO2+OH-=== HCO3—
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: 
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为_______________。在X极附近观察到的现象是________________。
②Y电极上的电极反应式为_________________,检验该电极反应产物的方法是___________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是__________,电极反应式为________________。
②Y电极的材料是__________,电极反应式为_______________。(说明:杂质发生的电极反应不必写出)
(10分)
(1)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应正极电极反应式为_______;放电时,CO32-移向电池的______(填“正”或“负”)极。
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
(3)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液c(H2CO3)______c(CO32-)(填“>”、“=”或“<”),原因是__________(用离子方程式和必要的文字说明)。
(1)通过NOx传感器可监测NOx的含量,固体体电解质可以传导O2-其工作原理示意图如下:
①Pt电极上发生的是 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式: 。
(2)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。
①导线中电子移动方向为________。(用A、D表示)
②生成目标产物的电极反应式为__________________。
③该储氢装置的电流效率η=____________________。(η= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
Ⅰ.已知可逆反应:M(g)+N(g)  P(g)+Q(g) ΔH>0,请回答下列问题:
P(g)+Q(g) ΔH>0,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为c(M)=1 mol·L-1,c(N)=2.4 mol·L-1。达到平衡后,M的转化率为60%,此时N的转化率为____________。
(2)若反应温度升高,M的转化率__________(填“增大”、“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4 mol·L-1,c(N)=a mol·L-1;
达到平衡后,c(P)=2 mol·L-1,a=____________。
Ⅱ.在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应
A(g) B(g)+C(g) △H=+85.1kJ·mol-1
B(g)+C(g) △H=+85.1kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h |
0 |
1 |
2 |
4 |
8 |
16 |
20 |
25 |
30 |
| 总压强p/100kPa |
4.91 |
5.58 |
6.32 |
7.31 |
8.54 |
9.50 |
9.52 |
9.53 |
9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为 。
平衡时A的转化率为_ ,列式并计算反应的平衡常数K 。
氯碱工业是最基本的化学工业之一,它的产品除应用于化学工业本身外,还广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。氯碱工业中制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制。学校实验小组精制粗盐水的实验过程如下:
请回答以下问题:
(1)操作a的名称是 ,所用玻璃仪器是 。
(2)在第Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为 溶液。
(3)判断加入试剂乙已过量的方法是 。
(4)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式 。
O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为 ,原子个数比为 ,分子的物质的量之比为 。
(2)等温等压下,等体积的氧气和臭氧所含分子个数比为 ,原子个数比为 ,质量之比为 。
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是 (用含NA的式子表示)。
(4)将8 g SO3加入Χg 水中,所形成的溶液里SO42-和水分子个数之比为1:5,则Χ等于 。
(5)常温常压下,14 g由N2和CO组成的混合气体中含有的原子数目为 。
选择下列实验方法分离物质,将分离方法的序号填在横线上:
A 过滤 B.结晶 C.分液 D.蒸馏 E.萃取分液 F.升华 G.渗析
(1) 分离水和苯的混合物;
(2) 分离饱和氯化钾溶液和沙子的混合物;
(3) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(4) 分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)的混合物;
(5) 从碘水中提取碘单质。
某些元素的性质或原子结构信息如下表所示(每空2分,共16分).:
| A(短周期) |
B(短周期) |
C |
D(短周期) |
| 原子最外层上p电子数等于次外层电子数 |
原子最外层有两个未成对电子,其单质为人类生存必需物质 |
单质为生活中常见的金属材料,有紫红色金属光泽 |
单质是常见的半导体材料,广泛应用于IT行业 |
(1)写出A单质与浓硝酸加热反应的化学方程式: 。
(2)写出B元素在周期表中的位置: ,
写出C元素基态原子的电子排布式: _。
(3)写出A与D的氧化物在高温下反应的化学方程式: _。
(4)写出B、D形成的化合物与NaOH溶液反应的离子方程式: 。
(5)比较A、B、D三种元素原子的第一电离能的大小 (由大到小用元素符号表示)。
(6)等电子原理——原子总数相同、价电子总数相同的粒子具有相似的化学键特征,它们的许多性质是相近的。写出二种由多个原子组成的含有与N3-电子数相同的粒子 (分子离子各一种)的化学式 、 。这些粒子空间构型为 。
试题篮
()