(本题共12分)元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
23、三氟化溴(BrF3)常用于核燃料生产和后处理,遇水立即发生如下反应:3BrF3 +5H2O → HBrO3 + Br2 + 9HF+ O2 。该反应中氧化剂与还原剂的物质的量之比为 ,每生成2.24 LO2(标准状况)转移电子数为 。
24、在食盐中添加少量碘酸钾可预防缺碘。为了检验食盐中的碘酸钾,可加入醋酸和淀粉-碘化钾溶液。看到的现象是 ,相应的离子方程式是 。
氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)  Cl2(aq) ---------------①
Cl2(aq) ---------------①
Cl2(aq)+ H2O  HClO + H+ +Cl------②
HClO + H+ +Cl------②
HClO  H+ + ClO- ---------------③
H+ + ClO- ---------------③
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
25、写出上述体系中属于电离平衡的平衡常数表达式:Ki = ,由图可知该常数值为 。
26、在该体系中c(HClO) + c(ClO-) c(H+)-c(OH-)(填“大于”“小于”或“等于”)。
27、用氯处理饮用水时,夏季的杀菌效果比冬季 (填“好”或“差”),请用勒夏特列原理解释 。
近年来大气问题受到人们越来越多的关注。按要求回答下列问题:
Ⅰ.实现反应CH4(g)+CO2(g) 2CO(g)+2H2(g),△H0,对减少温室气体排放和减缓燃料危机具有重要意义。在2L密闭容器中,通入5mol CH4与5mol CO2的混合气体,一定条件下发生上述反应,测得CH4的平衡转化率与温度、压强的关系如图。
2CO(g)+2H2(g),△H0,对减少温室气体排放和减缓燃料危机具有重要意义。在2L密闭容器中,通入5mol CH4与5mol CO2的混合气体,一定条件下发生上述反应,测得CH4的平衡转化率与温度、压强的关系如图。

则p1、p2、p3、p4由大到小的顺序 ,该反应的正反应是______(填“吸热”或“放热”)反应,当1000℃甲烷的转化率为80%时,该反应的平衡常数K=________。
Ⅱ.PM2.5污染与直接排放化石燃烧产生的烟气有关,化石燃料燃烧同时放出大量的SO2和NOx。
(1) 处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g) + 4NO2(g) =" 4NO(g)" + CO2(g) + 2H2O(g) △H1=-574kJ·mol-1
CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H2=-1160kJ·mol-1
CH4(g) + 2NO2 (g) = N2(g) + CO2(g) + 2H2O(g) △H3
则△H3= ,如果三个反应的平衡常数依次为K1、K2、K3,则K3=______(用K1、K2表示)
(2)实验室可用NaOH溶液吸收SO2,某小组同学在室温下,用pH传感器测定向20mL0.1mol·L-1NaOH溶液通入SO2过程中的pH变化曲线如图所示。

①ab段发生反应的离子方程式为________________。
②已知d点时溶液中溶质为NaHSO3,此时溶液中离子浓度由大到小的顺序为_______,如果NaHSO3的水解平衡常数Kh=1×10-12mol·L-1,则该温度下H2SO3的第一步电离平衡常数Ka=_________________。
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)原子序数为29的铜元素位于元素周期表中第周期。
(2)某青铜器中、
的质量分别为119
、20.7
,则该青铜器中
和
原子的数目之比为。
(3)研究发现,腐蚀严重的青铜器表面大都存在。关于
在青铜器腐蚀过程中的催化作用,下列叙述正确的是。
| A. | 降低了反应的活化能 | B. | 增大了反应的速率 |
| C. | 降低了反应的焓变 | D. | 增大了反应的平衡常数 |
(4)采用"局部封闭法"可以防止青铜器进一步被腐蚀。如将糊状涂在被腐蚀部位,
与有害组分
发生复分解反应,该化学方程式为。
(5)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是(填图中字母""或"
"或"
");
②环境中的扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
,其离子方程式为;
③若生成4.29 ,则理论上耗氧体积为
(标准状况)。
(15分)乙苯催化脱氢制苯乙烯反应:
(1)已知:
| 化学键 |
C-H |
C-C |
C=C |
H-H |
| 键能/kJ·molˉ1 |
412 |
348 |
612 |
436 |
计算上述反应的△H=________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=____________(用α等符号表示)。
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实___________。
②控制反应温度为600℃的理由是____________。
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有_________(填编号)。
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利于CO2资源利用
Ⅰ.(6分)请回答:
(1)H2O2的电子式___________。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由________________。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式_____________。
(4)完成以下氧化还原反应的离子方程式:
( )MnO4-+( )C2O42-+______=( )Mn2++( )CO2↑+________
Ⅱ.(12分)化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(1)甲的化学式__________。
(2)甲与AlCl3反应得到NaAlH4的化学方程式__________。
(3)NaAlH4与水发生氧化还原反应的化学方程式__________。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 。
(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。
判断该同学设想的制备和验纯方法的合理性并说明理由___________。
碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加
和
,即可得到
,该反应的还原产物为。
(2)上述浓缩液中含有
、
等离子,取一定量的浓缩液,向其中滴加
溶液,当
开始沉淀时,溶液中
为:,已知
=1.8×10-10,
=8.5×10-17。
(3)已知反应
的
,1
、1
分子中化学键断裂时分别需要吸收436
、151
的能量,则1
分子中化学键断裂时需吸收的能量为
。
(4)
研究了下列反应:

在716
时,气体混合物中碘化氢的物质的量分数
与反应时间
的关系如下表:
| 0 |
20 |
40 |
60 |
80 |
120 |
|
| 1 |
0.91 |
0.85 |
0.815 |
0.795 |
0.784 |
|
| 0 |
0.60 |
0.73 |
0.773 |
0.780 |
0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:。
②上述反应中,正反应速率为
正=
正·
,逆反应速率为
逆=
逆·
,其中
正、
逆为速率常数,则
逆为(以
和
正表示)。若
正 = 0.0027
,在
=40
时,
正=
③由上述实验数据计算得到
正~
和
逆~
的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为(填字母)

苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:


相关化合物的物理常数
| 物质 |
相对分子质量 |
密度( |
沸点/℃ |
| 异丙苯 |
120 |
0.8640 |
153 |
| 丙酮 |
58 |
0.7898 |
56.5 |
| 苯酚 |
94 |
1.0722 |
182 |
回答下列问题:
(1)在反应器中通入的
是。
(2)反应①和②分别在装置和中进行(填装置符号)。
(3)在分解釜中加入的
为少置浓硫酸,其作用是,优点是用量少,缺点是。
(4)反应②为(填"放热"或"吸热")反应。反应温度控制在50-60℃,温度过高的安全隐患是。
(5)中和釜D中加入的Z最适宜的是(填编号。已知苯酚是一种弱酸)。
a. b.
c.
d.
(6)蒸馏塔中的馏出物
和
分别为和,判断的依据是。
(7)用该方法合成苯酚和丙酮的优点是。
酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,,
和
等组成的糊状填充物,该电池在放电过程产生
,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(/100
水)

| 化合物 |
|||
| 10-17 |
10-17 |
10-39 |
回答下列问题:
(1)该电池的正极反应式为,电池反应的离子方程式为
(2)维持电流强度为0.5,电池工作五分钟,理论上消耗
。(已经
=96500
)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有和
,二者可通过分离回收;滤渣的主要成分是
、和,欲从中得到较纯的
,最简便的方法是,其原理是。
(4)用废电池的锌皮制备的过程中,需去除少量杂质铁,其方法是:加稀硫酸和
溶解,铁变为,加碱调节至
为时,铁刚好完全沉淀(离子浓度小于1×10-5
时,即可认为该离子沉淀完全);继续加碱调节至
为时,锌开始沉淀(假定
浓度为0.1
)。若上述过程不加
后果是,原因是。
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
高效,且腐蚀性小。请回答下列问题:
(1)净水的原理是。
溶液腐蚀钢铁设备,除
作用外,另一主要原因是(用离子方程式表示)。
(2)为节约成本,工业上用氧化酸性
废液得到
。
①若酸性废液中
=2.0×10-2
·
,
=1.0×10-3
·
,
=5.3×10-2
·
,则该溶液的
约为。
②完成氧化
的离子方程式:
+
+=
+
+
(3)在溶液中分三步水解:
+

+
+
![]()
+
+

+
以上水解反应的平衡常数、
、
由大到小的顺序是。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:+

欲使平衡正向移动可采用的方法是(填序号)。
.降温
.加水稀释
.加入NH4Cl
.加入
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以·
表示]的最佳范围约为
·
。
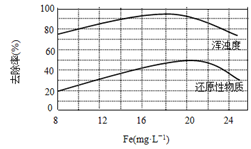
为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(铁主要以存在)转变成重要的化工原料
(反应条件略)。

活化硫铁矿还原的主要反应为:
,不考虑其他反应。请回答下列问题:
(1)第Ⅰ步与
反应的离子方程式是。
(2)检验第Ⅱ步中是否完全还原,应选择(填字母编号)。
A.溶液 B.
溶液 C.
溶液
(3)第Ⅲ步加调溶液
到5.8左右,然后在第Ⅳ步通入空气使溶液
降到5.2,此时
不沉淀,滤液中铝、硅杂质除尽。通入空气引起溶液
降低的原因是。
(4)可转化为
,
在空气中加热反应可制得铁系氧化物材料。
已知25℃,101时:
在空气中加热反应生成
的热化学方程式是。
(5)在一定条件下可制得
(二硫化亚铁)纳米材料。该材料可用于制造高容量锂电池,电池放电时的总反应为
,正极反应式是。
(6)假如烧渣中的铁全部视为,其含量为50%。将
质量分数为
%的硫酸加入到
烧渣中浸取,铁的浸取率为96%,其他杂质浸出消耗的硫酸以及调
后溶液呈微酸性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入
。
(12分)软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4·H2O ,反应的化学方程式为:MnO2+SO2=MnSO4
(1)质量为17.40g纯净MnO2最多能氧化_____L(标准状况)SO2。
(2)已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度小于1×10-6mol·L-1),需调节溶液pH范围为________。
(3)下图可以看出,从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为_______。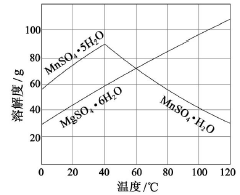
(4)准确称取0.1710gMnSO4·H2O样品置于锥形瓶中,加入适量H2PO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+,用c(Fe2+)=0.0500mol·L-1的标准溶液滴定至终点(滴定过程中Mn3+被还原为Mn2+),消耗Fe2+溶液20.00mL。计算MnSO4·H2O样品的纯度(请给出计算过程)
研究在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的主要以4种无机碳形式存在,其中
占95%,写出
溶于水产生
的方程式:。
(2)在海洋循环中,通过下图所示的途径固碳。

①写出钙化作用的离子方程式:。
②同位素示踪法证实光合作用释放出的只来自于
,用
标记物质的光合作用的化学方程式如下,将其补充完整:+=
+
+
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收,用
从酸化后的还说中吹出
并用碱液吸收(装置示意图如下),将虚线框中的装置补充完整并标出所用试剂。

②滴定。将吸收液洗后的无机碳转化为,再用
溶液滴定,消耗
溶液,海水中溶解无机碳的浓度=
。
(4)利用下图所示装置从海水中提取,有利于减少环境温室气体含量。

①结合方程式简述提取的原理:。
②用该装置产生的物质处理室排出的海水,合格后排回大海。处理至合格的方法是。
氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
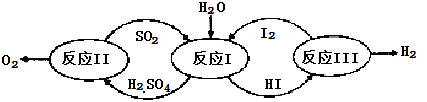
(1)反应Ⅰ的化学方程式是。
(2)反应Ⅰ得到的产物用进行分离。该产物的溶液在过量
的存在下会分成两层--含低浓度
的
层和高浓度的
的
层。
①根据上述事实,下列说法正确的是(选填序号)。
a.两层溶液的密度存在差异
b.加前,
溶液和HI溶液不互溶
c.在
溶液中比在
溶液中易溶
②辨别两层溶液的方法是。
③经检测,层中
=2.06:1。其比值大于2的原因是。
(3)反应Ⅱ:
它由两步反应组成:i.
ii.分解。
L(L1、L2),X可分别代表压强或温度。下图表示L一定时,ii中的平衡转化率随X的变化关系。
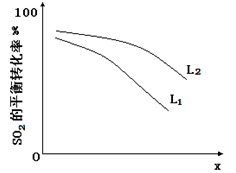
①X代表的物理量是。
②判断L1、L2的大小关系,并简述理由:。
(一) 尿素又称碳酰胺,是含氮量最高的氮肥,工业上利用二氧化碳和氨气在一定条件下合成尿素。其反应分为如下两步:
第一步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵)(l) △H1= -330.0 kJ·mol-1
H2NCOONH4(氨基甲酸铵)(l) △H1= -330.0 kJ·mol-1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2=" +" 226.3 kJ·mol-1
H2O(l)+H2NCONH2(l) △H2=" +" 226.3 kJ·mol-1
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 m3 密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定。
②反应进行到10 min时测得CO2的物质的量如上图所示,则用CO2表示的第一步反应的速率v(CO2)= mol/(L·min)。
③当反应在一定条件下达到平衡,若在恒温、恒容下再充入一定量气体He,则CO(NH2)2(l)的质量_________(填“增加”、“减小”或“不变”)。
(二)氨是制备尿素的原料,NH3、N2H4等在工农业生产、航空航天等领域有广泛应用。
氨气溶于水得到氨水,在25℃下,将amol/L的氨水与bmol/L的硫酸以3∶2体积比混合反应后溶液呈中性。用含a和b的代数式表示出氨水的电离平衡常数为_________。
(三)氢气是合成氨的原料。“氢能”将是未来最理想的新能源。
(1)在25℃,101KPa条件下,1 g氢气完全燃烧生成液态水时放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为 。
(2)氢气通常用生产水煤气的方法制得。其中C(s)+ H2O(g) CO(g)+H2(g),在850℃时平衡常数K=1。若向1升的恒定密闭真空容器中同时加入x mol C和6.0mol H2O。
CO(g)+H2(g),在850℃时平衡常数K=1。若向1升的恒定密闭真空容器中同时加入x mol C和6.0mol H2O。
①当加热到850℃反应达到平衡的标志有______________ 。
| A.容器内的压强不变 |
| B.消耗水蒸气的物质的量与生成CO的物质的量相等 |
| C.混合气的密度不变 |
| D.单位时间有n个H-O键断裂的同时有n个H-H键断裂 |
②x应满足的条件是 。
(四)CO2是合成尿素的原料,但水泥厂生产时却排放出大量的CO2。华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示: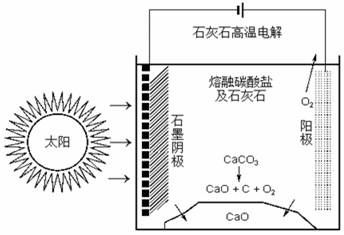
(1)上述生产过程的能量转化方式是 。
(2)上述电解反应在温度小于900℃时进行碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为 ,阴极的电极反应式为 。
【化学一选修2:化学与技术】(15分)三氧化二镍(Ni2O3)是一种重要的蓄电池材料。工业上利用镍废料(镍、铁、钙、镁合金为主)制取草酸镍晶体(NiC2O4-2H2O),再高温煅烧草酸镍晶体制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。下列工艺流程示意图如下;
回答下列问题
(1)为提高酸溶操作中镍废料的转化率,可采取的措施有答出三条 。
(2)加入H2O2发生的主要反应的离子方程式为 。
(3)加入NH4F后除掉的杂质是____
(5)工业上还可用电解法制取Ni2O3。用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2S04后采用惰性电极电解。电解过程中产生的Cl2有80%在弱碱性条件下生成ClO—,再把二价镍氧化为三价镍。当amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为____。电解法制取Ni203的实际过程中,先获得一种结晶水合物,己知含1 mol Ni的诙结晶水合物中含有0.5 mol结晶水。取该化合物20.2 g进行充分加热,获得Ni203固体和0.2 mol水,则该结晶水合物的化学式为 .
试题篮
()