现有一包5g固体混合物,可能含有Zn、ZnO、Zn(OH)2、ZnCO3.将其加入到10%的稀硫酸中,固体混合物全部溶解,消耗的稀硫酸为49g,则混合物中肯定含有的物质是( )
A.ZnB.ZnOC.Zn(OH)2D.ZnCO3
控制变量法是实验探究的重要方法,下列实验方法的设计中,能达到实验目的是()

| A. | 图甲比较铁、铜的金属活动性强弱 |
| B. | 图乙探究金属的锈蚀是否需要水 |
| C. | 图丙探究 对 分解的催化作用 |
| D. | 图丁探究可燃物的燃烧是否需要达到一定温度 |
某气体可能含有H2、CO、N2、CH4中的一种或几种,点燃该气体后,在火焰上方罩一只冷而干燥的烧杯,烧杯内壁有小水珠出现;把烧杯迅速翻转,注入少量澄清的石灰水,振荡,石灰水变浑浊。则该气体成分不可能是
| A.CO和 CH4 | B.H2和CO | C.CH4 | D.H2和N2 |
实验室有一包白色固体,其中除了碳酸钠以外,还可能含有硝酸钡、硫酸钠、氢氧化钠中的一种或几种。为确定其组成进行如下实验:①取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解;②继续向烧杯中逐滴加入足量稀硝酸并不断搅拌,此时固体质量变化如图。下列说法正确的是( )

A.A→B段对应的实验现象是固体部分溶解,无气泡冒出
B.B→C段对应溶液pH逐渐变大
C.原白色固体中一定含有碳酸钠、硫酸钠、硝酸钡
D.C点对应溶液中一定含有的溶质是硝酸、硝酸钠、碳酸钠、硝酸钡
某固体可能含有CaCl 2、Na 2SO 4、CuSO 4、KNO 3、Na 2CO 3中的一种或几种,现对其进行如下实验:
①取少量固体于试管中,加适量蒸馏水,固体完全溶解得透明溶液;
②在①所得溶液中,滴加足量BaCl 2溶液,产生白色沉淀。过滤后,在白色沉淀中加过量稀盐酸,沉淀部分溶解,且有气泡产生。
下列对原固体成分的说法正确的是( )
| A. |
一定有Na 2CO 3和Na 2SO 4,可能有KNO 3、CuSO 4、CaCl 2 |
| B. |
一定有Na 2CO 3,Na 2SO 4和CuSO 4两种物质中至少有一种 |
| C. |
一定有Na 2CO 3和Na 2SO 4,不含CaCl 2,可能有KNO 3、CuSO 4 |
| D. |
一定有Na 2CO 3和Na 2SO 4,不含CuSO 4和CaCl 2,可能有KNO 3 |
下列方法中能鉴别出空气、氧气、二氧化碳等三瓶无色气体的是
| A.用蘸有澄清石灰水的烧杯 | B.闻气体的气味 |
| C.分别将燃着的小木条伸入三瓶气体中 | D.以上方法都不行 |
实验是人们认识物质的重要手段,关于下列四个实验的论述错误的是
 |
 |
 |
 |
| 玻璃棒的作用是引流 |
酸类物质具有相似的化学性质,但由于酸根离子不同,其性质也存在差异 |
通过对比蜡烛在空气中燃烧的现象得出:反应物的浓度影响反应的速率 |
导管的长度对蒸馏效果没有影响 |
郝颖同学在化学课上提出,可用澄清石灰水来检验人呼出的气体是否是二氧化碳气体,就这一过程而言,属于科学探究环节中的
| A.建立假设 | B.收集证据 | C.设计实验 | D.做出结论 |
有一包不纯的碳酸钾粉末,所含杂质可能是硝酸钾、硝酸钙、氯化钾、氯化亚铁、碳酸钠中的一种或几种。为确定其成分,进行如下实验:
(1)取少量该粉末于试管中,加足量的水充分溶解,得到无色澄清溶液。向该溶液中加入适量的硝酸银溶液,有白色沉淀产生,再加入足量的稀硝酸,充分反应后,部分白色沉淀消失。
(2)另取13.8g该粉末于烧杯中,加水使其完全溶解,再加入200g一定溶质质量分数的氯化钡溶液,恰好完全反应,生成19.7g白色沉淀。
(资料:稀硝酸与碳酸盐能发生复分解反应,稀硝酸与氯化银不反应)
下列说法正确的是( )
A.杂质中一定不含有氯化亚铁
B.杂质中一定含有氯化钾,可能含有硝酸钾、碳酸钠
C.该包粉末的组成只有两种情况
D.所用氯化钡溶液中溶质的质量分数为20.8%
某白色粉末可能由碳酸钠、氯化钠、氢氧化钠、氯化钡中的一种或几种组成,为确定其组成,某同学进行如下实验:实验一:取该固体适量加入水,得到浑浊液体,过滤;实验二:取实验一所得滤液少许于试管中,加入过量氯化钡溶液,振荡,静置后滴加酚酞溶液,溶液变红。下列判断正确的是( )
A.该白色粉末中不含氯化钡
B.该白色粉末中含有氢氧化钠
C.该白色粉末中一定没有氯化钠
D.实验二中氯化钡改成氢氧化钡对实验无影响
下列说法不正确的有( )
①除去二氧化碳中混有的少量氧气,可以通入一氧化碳后点燃,将氧气转化为二氧化碳
②实验室用6%的氯化钠溶液配制3%的氯化钠溶液,量取6%的氯化钠溶液时俯视读数,若其他操作均正确,则所配溶液中溶质的质量分数大于3%
③某固体可能由氯化钠、硫酸钠、氯化钡、氯化镁、硫酸钾中的一种或几种组成,取少量该固体,加入足量的稀氢氧化钠溶液,产生白色沉淀,过滤,向沉淀中加入足量稀硝酸,沉淀部分溶解,则该固体的组成有5种情况
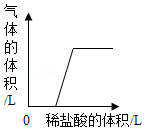
④某碳酸钠溶液中可能含有另一种溶质,取一定量该溶液,逐滴滴加稀盐酸,产生气体的体积与加入稀盐酸的体积关系如图所示,则该碳酸钠溶液中一定含有氢氧化钠。
A.1种B.2种C.3种D.4种
现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验。下列判断正确的是( )

A.无色溶液B的溶质只有硝酸钙
B.该实验中涉及的基本反应类型不止一种
C.原溶液中的杂质只有氯化钙
D.原溶液中的杂质可能由氯化钙、硝酸钙、氯化钠组成
小明设计了趣味实验装置(见下图),其气密性良好。若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是
| A.硝酸铵和水 | B.氯化钠和水 |
| C.二氧化锰和过氧化氢溶液 | D.铜和稀盐酸 |
有一包固体样品,可能由氢氧化钠、硫酸钠、硝酸镁、硝酸铜、碳酸钙中的一种或几种物质组成。为确定该样品的组成,某兴趣小组同学取适量样品进行探究。探究过程如图:

根据以上信息判断,下列说法正确的是( )
| A. |
白色沉淀a的成分是碳酸钙 |
| B. |
该样品中一定存在氢氧化钠、硝酸镁、硫酸钠、碳酸钙,一定不存在硝酸铜 |
| C. |
该样品中一定存在硫酸钠、碳酸钙、硝酸镁,一定不存在硝酸铜和氢氧化钠 |
| D. |
若步骤①②保持不变,用硝酸钡溶液代替步骤③中的氢氧化钡溶液,则不需要进行步骤④的探究,也能确定该样品的组成 |
试题篮
()