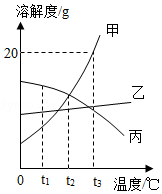
如图是甲、乙、丙三种固体物质的溶解度曲线.回答相关问题
(1)t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比为 .
(2)t2℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是 (用“甲”、“乙”、“丙”及“>”、“<”或“=”表示).
(3)将t3℃的甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,所得溶液的质量最大是 (用“甲”、“乙”、“丙”填空).
(4)现有甲、乙混合物溶液,需要从混合物溶液中提纯乙固体,采用的方法有(写出一种即可) .
已知NH4Cl、KNO3在不同温度时的溶解度
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度/g |
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
|
请回答下列问题:
(1)在35℃时,KNO3的溶解度 NH4Cl的溶解度。(填“>”或“=”或“<”)
(2)若KNO3固体中含有少量NH4Cl固体,可采用 获得KNO3晶体。(填“蒸发结晶”或“降温结晶”)
(3)25℃时,将15克KNO3固体溶解在50克水中,所得溶液为 。(填“饱和溶液”或“不饱和溶液”)
(4)20℃时,饱和NH4Cl溶液溶质质量分数为 。(精确到0.1%)
几种物质在不同温度时的溶解度如下表所示:
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度 /g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
38.4 |
KCl |
27.6 |
31.0 |
34.0 |
34.7 |
40.0 |
42.6 |
45.5 |
48.3 |
51.1 |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
|
KNO3 |
14.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
|
请回答下列问题:
(1)20℃时,上述四种物质中溶解度最大的是 (填化学式,下同)。
(2)将温度为80℃、质量相同的上述四种物质的饱和溶液分别降温到20℃,析出 晶题体最多的是 。
(3)在某温度范围内NaCl和KCl的溶解度可能相等,该温度范围是 (填字母序号)。
A.10℃~20℃
B.20℃~30℃
C.30℃~40℃
D.40℃~50℃
(4)20℃时将20 gNaCl加入50g水中,充分溶解后所得溶液中溶质的质量分数是 (计算结果精确至 0.1%)。
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
(1)t3℃时,甲、乙、丙三种物质的溶解度大小关系是 (用“甲”、“乙”,“丙”及“>”、“<”或“=”表示);
(2)t2℃时,乙物质的饱和溶液中溶质、溶剂的质量之比为 (填最简整数比)。
(3)欲配制相同质量分数的乙,丙饱和溶液,应保持温度在 ℃;
(4)将t3℃时甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,所得溶液质量的大小关系是 (用“甲”、“乙”,“丙”及“>”“<”或“=”表示)。

甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题:
(1)P点表示的含义是 。
(2)t1℃时,将甲的不饱和溶液转化为该温度下饱和溶液的一种方法是 。
(3)t3℃时将90g甲的饱和溶液降温至t1℃,析出晶体的质量是 g。
(4)t3℃时,将等质量的三种物质的饱和溶液降温到t2℃,对所得溶液的叙述正确的是 (填字母序号)。
A.丙溶液的溶质质量分数不变 B.溶剂的质量关系是甲=乙>丙 C.溶液的质量关系是丙>乙>甲

如图是A、B、C三种固体物质的溶解度曲线。
(1)P点表示的含义是 。
(2)t1℃时,将35gA物质加入到50g水中,形成 (填“饱和”或“不饱和”)溶液。
(3)B中混有少量的A,提纯B的方法是 。
(4)将等质量的A、B、C三种固体物质分别配成t3℃时的饱和溶液,所得溶液的质量最多的是 。
(5)将t1℃时A、B、C三种物质的饱和溶液升温到t3℃时,所得溶液的溶质质量分数由大到小的关系是 。

硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答。
温度/℃ |
20 |
40 |
60 |
80 |
100 |
|
溶解度/g |
硝酸钾 |
31.6 |
63.9 |
110 |
169 |
246 |
氯化钠 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
|
(1)60℃时硝酸钾的溶解度是 g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是 。
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。
①烧杯A中溶解的物质是 。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数 (填“变大”、“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量 (填“一定”或“不一定”)相等。

利用溶解度曲线,可以获得许多有关物质溶解度的信息。如图是a、b、c三种物质的溶解度曲线。请回答下列问题:
(1)t3℃时,a、b、c三种物质溶解度由大到小的顺序是 。
(2)P点的含义 。
(3)将t1℃时a、b、c三种物质的饱和溶液升温到t2℃(不考虑水蒸发),所得溶液溶质质量分数由大到小的顺序是 。
(4)下列说法不正确的是 (填字母序号)。
A.将t3℃时等质量的a、b两种物质的饱和溶液降温到t2℃,析出晶体的质量a>b
B.t3℃时,配制溶质质量分数为50%的a溶液
C.将t3℃时a、b、c三种物质的饱和溶液各100g降温到t1℃,溶液中溶剂的质量为b<a=c

A、B、C三种物质的溶解度曲线如图。请回答下列问题。
(1)t1℃时,A物质的溶解度是 g。
(2)保持温度不变将B的不饱和溶液转化为饱和溶液,可采用的一种方法是 。
(3)将t2℃时等质量A、B、C三种物质的饱和溶液降温至t1℃,所得溶液中溶剂质量最少的是 。
(4)t1℃时将A、B、C三种物质各5g分别加入20g水中充分溶解,所得溶液质量的大小关系为 。

如图为a、b、c三种不含结晶水的固体物质在水中的溶解度曲请回答下列问题:
(1)t1℃时,a、b、c三种物质溶解度由大到小的顺序为 。
(2)当b中混有少量a时,提纯b的方法是 。
(3)t4℃时,将等质量的a、b、c三种饱和溶液降温到t3℃时,所得溶液中,溶剂质量由大到小的顺序为 。
(4)t4℃时,在三个装有50g水的烧杯中分别加入a、b、c三种物质各20g,能形成不饱和溶液的是 ,再降温到t2℃时,所得三种溶液的溶质质量分数大小关系为 。

a、b、c三种固体物质的溶解度曲线如图所示,回答下列问题:
(1)M点的含义是 。
(2)在t2℃时,向盛有50ga物质的烧杯中加入80g水,充分溶解后,所得溶液的质量为 g。
(3)在t1℃时,将a、b、c三种物质的饱和溶液分别升温至t2℃,所得三种溶液溶质的质量分数由大到小的顺序是 。
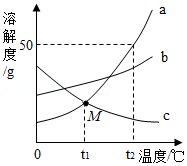
A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:
(1)t2℃时,A、B、C三种物质溶解度的大小关系是 (用“A、B、C”和“>、<、=”表示)
(2)要使接近饱和的C溶液在保持溶质质量分数不变的情况下变成饱和溶液的方法是 。
(3)将100g质量分数为30%的A溶液由t3℃降温至t1℃,降温后所得溶液中溶质的质量分数是 。
(4)t3℃时,A、B、C三种物质的混合溶液中,A、B、C三种溶质的质量相等,将混合溶液在该温度下恒温蒸发溶剂,首先析出的物质是 。

硝酸钾的溶解度曲线如图所示。
(1)30℃时,硝酸钾的溶解度是 。
(2)60℃时,在200g水中加入120g硝酸钾固体,充分搅拌。
①所得溶液是 (填“饱和”或“不饱和”)溶液。
②将上述溶液降温至30℃,可析出硝酸钾晶体 g,此时溶液的溶质质量分数 (填“>”、“=”或“<”)45.8%。

溶液在生活、生产中具有广泛的用途。
(1)在20℃时,将20g氯化钾固体加入50g水中,充分搅拌后,仍有3g氯化钾固体未溶解。所得溶液中氯化钾的质量分数为 (计算结果保留一位小数);20℃时氯化钾的溶解度为 。
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图。t1℃时,甲溶液的溶质质量分数与乙溶液的溶质质量分数相比,前者与后者的关系是 (填字母)。
A.大于 B.小于 C.等于 D.无法确定
(3)如图是实验室稀释浓硫酸的正确和错误操作,请说明不能将水直接倒入浓硫酸中进行稀释的原因 。


试题篮
()