类比推理在化学学习和科学研究中有重要意义。下列类比推理正确的是( )
A.NaOH和KOH都是强碱,两者都能与硫酸铜溶液反应生成蓝色沉淀
B.N2和O2都是非金属单质,两者的化学性质都非常活泼
C.盐酸和硫酸都是强酸,两者都易挥发
D.CaO和Fe2O3都是金属氧化物,两者都能与水反应生成碱
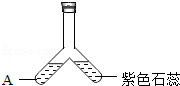
如图所示装置中观察到紫色石蕊变红。
(1)物质A是 (选填序号)。
a.浓氨水 b.浓硫酸 c.浓盐酸
(2)该实验现象说明构成物质的微粒是 。
盐酸是重要化工产品。
(1)盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式 。
(2)盐酸具有挥发性,在空气中打开盛有浓盐酸的试剂瓶瓶盖,在瓶口处观察到的现象是 。
(3)氨水也具有挥发性,可挥发出氨气。如图,在 a、b 处放有浸泡过浓盐酸或浓氨水的棉花,过一会在 c 处可观察到的现象是 ,a 处是放有浸泡过 的棉花。(已知:①NH3 与 HCl 在空气中相遇可反应生成白色固体 NH4Cl;②相对分子质量越小的气体扩散速度越快)
(4)实验室可用NH4Cl 与Ca(OH)2 固体加热发生复分解反应制取 NH3,请写出此反应的化学方程式 ,收集 NH3可用向 排 空气法。

判断下列大小或强弱关系,并用“<”、“>”或“=”填空。
(1)金属活动性:锌 铜;
(2)受热稳定性:碳酸钙 碳酸氢铵;
(3)相同条件下的密度:空气 二氧化碳;
(4)相同条件下的挥发性:稀盐酸 浓盐酸。
下列有关物质的性质与用途具有对应关系的是( )
A.氢气密度小,可用作清洁能源
B.酒精具有可燃性,可用作溶剂
C.浓硫酸具有吸水性,可用作干燥剂
D.二氧化碳不支持燃烧,干冰可用作制冷剂
如图所示,电子秤上的量筒中分别盛有蒸馏水、浓硫酸,放置一段时间。
(1)A中示数变小,从微粒的角度解释其原因是 。
(2)B中示数变大,说明浓硫酸具有 。

下列关于物质用途的说法中,错误的是( )
A.亚硝酸钠用于烹调
B.盐酸用于金属表面除锈
C.碳酸氢钠用于培制糕点
D.熟石灰用于改良酸性土壤
下列事例,用化学知识解释正确的是( )
A.用食醋清除水垢,是利用了食醋的酸性
B.在空气中铝比铁耐腐蚀,是因为铝不与空气中氧气反应
C.家用净水器内部含大量的活性炭,是利用了活性炭的杀菌作用
D.把可燃物粉碎后燃烧效率更高,是因为粉碎后降低了可燃物的着火点
下列归纳总结完全正确的一组是( )
A.化学之最 |
B.化学与生活 |
①熔点最低的金属是汞 ②地壳中含量最高的金属元素是铁 ③天然存在的最硬的物质是金刚石 |
①衣服上的油污:可用汽油除去 ②水壶中的水垢:可加食盐水浸泡除去 ③冰箱中的异味:可放活性炭吸附 |
C.物质保存方法及解释 |
D.化学与工农业 |
①浓盐酸密封保存:防止挥发 ②白磷在冷水中保存:隔绝空气 ③氢氧化钠密封保存:防止潮解、变质 |
①用焦炭和铁矿石炼铁 ②用石油产品生产合成纤维 ③施用过量化肥,农药增加粮食产量 |
A.AB.BC.CD.D
现有①硝酸钾②氯化钾③浓盐酸④浓硫酸⑤钨⑥铁,选择适当的物质填空.
(1)属于复合肥料的是 (填序号,下同);
(2)敞口放置在空气中质量减小的是 ;
(3)熔点最高的金属是 .
下列有关硫酸的认识或做法,正确的是( )
| A. |
组成:硫酸溶液中H +和SO 4 2 ﹣的数目相同 |
| B. |
性质:能与CO 2、SO 2等非金属氧化物反应 |
| C. |
用途:用于生产化肥、农药、火药、染料等 |
| D. |
生产:含硫酸的工业废水,用CaCl 2处理后直接排放 |
下列有关物质的性质与用途对应关系不成立的是( )
A.纯氧无色无味,常用于医疗急救
B.熟石灰有碱性,用于改良酸性土壤
C.盐酸具有酸的通性,用于金属表面除锈
D.氦气密度比空气小,化学性质不活泼,用于填充庆典气球
通过实验以及对实验现象的观察、记录和分析,可以发现和验证化学原理。下面是小兰同学在完成酸、碱的性质实验时记录的部分实验现象,其中正确的是( )
A.打开盛有浓盐酸的试剂瓶瓶盖,瓶口有白烟产生
B.向氧化铁中加入足量稀硫酸,红棕色固体溶解,溶液由无色变成浅绿色
C.向氯化铜溶液中加入几滴氢氧化钠溶液,产生蓝色沉淀
D.向氢氧化钙溶液中加入几滴紫色石蕊溶液,石蕊溶液由紫色变成红色
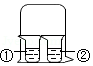
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
选项 |
①中的物质 |
②中的物质 |
预测①中的现象 |
A |
紫色石蕊试液 |
浓氨水 |
溶液由紫色变为蓝色 |
B |
氢氧化钡溶液 |
浓硫酸 |
有白色沉淀 |
C |
硫酸铜溶液 |
浓氨水 |
有蓝色沉淀 |
D |
硝酸银溶液 |
浓盐酸 |
有白色沉淀 |
A.AB.BC.CD.D
试题篮
()