同学要通过实验来测定某品牌的纯碱样品中Na2CO3的质量分数。他们取了6g纯碱样品放入烧杯中,再将80g一定溶质质量分数的稀盐酸分4次加入该烧杯中,充分反应后测得实验数据如下表(不考虑CO2溶解于水)。
实验次数 |
1 |
2 |
3 |
4 |
加入稀盐酸的质量/g |
20 |
20 |
20 |
20 |
烧杯中剩余物质的质量/g |
25.2 |
m |
63.8 |
83.8 |
(1)表格中m的值为 。
(2)样品中Na2CO3的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
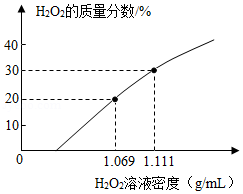
在新冠肺炎的疫情防控中,过氧化氢(H2O2)广泛用于环境消毒,在放置过程中会缓慢分解。某单位有一桶未曾使用过的久置的H2O2溶液,观测得其溶液密度为1.069g/mL,该温度下溶液的密度和溶质质量分数的对应关系如图。桶上标签提供的信息:①H2O2的质量分数为30%;②内装溶液质量50kg,完成下列问题:
(1)该久置的H2O2溶液的溶质质量分数为 。
(2)若用此久置的H2O2溶液来配制质量分数为3%的环境消毒液200kg,需用这种H2O2溶液 kg。
(3)若这桶H2O2溶液放置至完全分解,桶中剩下的液体质量是多少?(假设液体不挥发,通过计算回答,结果精确到0.1)
“84消毒液”是一种常用含氯消毒用品,有效成分是次氯酸钠(NaClO)。使用时,可根据实际需求进行配比,并规范使用,以防引发危险。
(1)“84消毒液”中的有效氯来自次氯酸钠,计算次氯酸钠中氯元素的质量分数。(计算结果精确到0.1%)
(2)现需要5L有效氯浓度为500mg/L的稀溶液,选用有效氯浓度为50000mg/L的某品牌“84消毒液”进行配制,需加水多少升?( 忽略混合前后溶液体积的变化)
(3)“84消毒液”不能与洁厕灵混合使用,因为“84消毒液”里的次氯酸钠与洁厕灵里的盐酸会发生化学反应,产生的氯气对人体有害,不同浓度氯气对人体的影响如表所示。
浓度(mg/m3) |
对人体的影响 |
3000 |
可立即麻痹呼吸中枢,导致瞬间死亡 |
120﹣170 |
极为危险,会引起急性肺水肿及肺炎 |
40﹣60 |
在1小时内便可致人严重中毒 |
通过计算分析,在10米3密闭空间里,若将1.49克次氯酸钠与盐酸完全反应,产生的氯气会对人体造成怎样的影响?(次氯酸钠与盐酸反应的化学方程式为:NaClO+2HCl═NaCl+Cl2↑+H2O)
白铜(Cu﹣Ni)是工业上常用的一种合金,金属镍(Ni)的金属活泼性与铁相似,且化合价显+2价。为测定20g某白铜样品中镍的质量,设计了如下实验:

试问:
(1)将白铜研碎的目的是 。
(2)白铜样品中镍的质量 g。
(3)所用稀硫酸中溶质的质量分数(写出计算过程)。
"84消毒液"是一种常用含氯消毒用品,有效成分是次氯酸钠(NaClO)。使用时,可根据实际需求进行配比,并规范使用,以防引发危险。
(1)"84消毒液"中的有效氯来自次氯酸钠,计算次氯酸钠中氯元素的质量分数。(计算结果精确到0.1%)
(2)现需要5L有效氯浓度为500mg/L的稀溶液,选用有效氯浓度为50000mg/L的某品牌"84消毒液"进行配制,需加水多少升?( 忽略混合前后溶液体积的变化)
(3)"84消毒液"不能与洁厕灵混合使用,因为"84消毒液"里的次氯酸钠与洁厕灵里的盐酸会发生化学反应,产生的氯气对人体有害,不同浓度氯气对人体的影响如表所示。
| 浓度(mg/m 3) |
对人体的影响 |
| 3000 |
可立即麻痹呼吸中枢,导致瞬间死亡 |
| 120﹣170 |
极为危险,会引起急性肺水肿及肺炎 |
| 40﹣60 |
在1小时内便可致人严重中毒 |
通过计算分析,在10米 3密闭空间里,若将1.49克次氯酸钠与盐酸完全反应,产生的氯气会对人体造成怎样的影响?(次氯酸钠与盐酸反应的化学方程式为:NaClO+2HCl═NaCl+Cl 2↑+H 2O)
某袋装食品的脱氧剂由活性炭、铁粉和食盐混合而成,三者质量比为2:2:1.现用该脱氧剂进行实验,回答下列问题:
(1)将该脱氧剂加入盐酸中,发生反应的化学方程式为 。
(2)打开失效的脱氧剂小袋,发现里面出现了红褐色物质,该物质的主要成分是 (填化学式)。5.0g未经使用的该脱氧剂最多能够吸收氧气 g。
(3)用电子秤称取7.20g完全失效后的脱氧剂放入烧杯中,加入足量稀硝酸,充分溶解后过滤,滤渣为黑色粉末。向所得滤液中加入足量AgNO3溶液,充分反应产生的沉淀质量为2.87g。列式计算该失效脱氧剂中NaCl的质量分数(计算结果精确到0.1%)。
为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有146g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为162.2g。计算:
(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数;
(3)反应后所得溶液中溶质的质量分数(结果精确至0.1%)。
某实验小组为测定铜和氧化铜的混合物中铜元素的含量,取20g该固体混合物,向其中逐滴加入稀H2SO4,测得剩余固体的质量与加入稀H2SO4的质量关系如图所示。回答下列问题:

(1)写出滴加稀H2SO4时发生反应的化学方程式 。
(2)该固体混合物中铜元素的质量为 。
(3)计算稀H2SO4中溶质的质量分数(写出计算过程)。
取氯化钡和盐酸的混合溶液100g于烧杯中,向其中滴加碳酸钠溶液,产生气体或沉淀的质量与加入的碳酸钠溶液质量的关系如图所示,请回答:
(1)产生沉淀的质量为 g。
(2)x的值为 。
(3)求所用碳酸钠溶液中溶质的质量分数(请写出计算过程)。

菱镁矿中主要含MgCO3、FeCO3和SiO2.以菱镁矿为原料制取镁的工艺流程如图。
回答下列问题:
(1)菱镁矿属于 (选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是 。
(3)写出菱镁矿中MgCO3与稀HCl反应的化学方程式 。
(4)溶液b→溶液c反应的化学方程式为:4FeCl2+ +4HCl=4FeCl3+2H2O(补充完方程式)
(5)溶液c调pH使Fe3+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8﹣ 。
已知:物质沉淀的pH见下表:
物质 |
Mg(OH)2 |
Fe(OH)3 |
开始沉淀的pH |
8.9 |
1.5 |
完全沉淀的pH |
10.9 |
2.8 |
(6)结合流程中的数据计算。
①菱铁矿中镁元素的质量分数为 (不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量(写出计算过程)。
小嘉发现:向碳酸钠溶液中倾倒稀盐酸,很快就产生了气泡:向碳酸钠溶液中逐滴加入稀盐酸,滴加一定量后才有气泡产生。查阅资料:向碳酸钠溶液中逐滴加入稀盐酸,先发生的反应是Na2CO3+HCl═NaCl+NaHCO3;当Na2CO3全部转化成NaHCO3后,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑。为此他用如图所示装置进行了如下实验:
步骤一:在广口瓶中加入10克溶质质量分数为10.6%的碳酸钠溶液,用注射器向瓶中缓慢注入一定量的溶质质量分数为7.3%的稀盐酸,观察到瓶内无明显现象; 步骤二:继续用注射器向瓶中注入稀盐酸,一段时间后观察到瓶内连续产生气泡,烧杯中澄清石灰水?。 |
(1)步骤二中,观察到烧杯中澄清石灰水 。
(2)上述实验中,加入稀盐酸多少克后,才开始产生二氧化碳? 。
(3)向一定量碳酸钠溶液中无论是倾倒还是逐滴加入足量的稀盐酸,完全反应后产生二氧化碳质量是相同的,其本质原因是什么? 。

某兴趣小组在实验室发现盛有固体氢氧化钠的试剂瓶破裂瓶盖处有"白毛"状物质(如图),根据所学知识,他们推断"白毛"状固体物质中含有碳酸钠,依据是 。他们取5g白色固体,加水配成20g溶液倒入烧杯中,将40g氯化钡溶液分成四等份,分4次加入烧杯中,充分反应后测得数据如下表:
| 实验次数 |
1 |
2 |
3 |
4 |
| 加入氯化钡溶液的质量/g |
10 |
10 |
10 |
10 |
| 烧杯中所得溶液的质量/g |
28.03 |
36.06 |
44.09 |
54.09 |
(1)第 次实验,加入的氯化钡与碳酸钠恰好完全反应。
(2)求5g白色固体中碳酸钠的质量。(写出计算过程,结果保留两位小数)

实验室用含杂质的锌(也称粗锌)与盐酸反应制取氢气,取8.0g含杂质的锌粒于烧杯中(所含杂质不溶于水,也不与酸反应),向其中加入73.0g稀盐酸,恰好完全反应后烧杯内剩余物质的质量为80.8g。计算:
(1)生成氢气的质量 g。
(2)求稀盐酸的溶质质量分数(请写出计算过程)。
某炼钢厂每天需消耗5000t含Fe2O376%的赤铁矿,该厂理论上可日产含Fe 98%的生铁的质量是多少?
试题篮
()