化学泡沫灭火器是常用灭火器之一,其反应原理为: 。现将34.2kg质量分数为10%的 溶液与270kg 溶液混合,恰好完全反应(假设生成的气体全部逸出)。
已知相对分子质量: 342; 142; 78。
试计算:
(1) 中O元素与S元素的质量比为 。
(2)最后所得溶液中 的质量分数。
(3)将34.2kg 溶液的溶质质量分数由10%变为20%可以用不同方法。请选择一种方法进行计算(只写出计算过程,不答具体操作)。
我国核工业技术世界领先,现已出口到西方发达国家。极硬的陶瓷材料碳化硼( )可用作核反应堆的中子吸收剂,还可用于制造坦克装甲、防弹背心等。在电弧炉中用C与 反应制得 ,反应的化学方程式为 。按此反应,当消耗70千克 时,可制得 多少千克?
某化肥厂生产的一种化肥包装袋上的部分说明如图所示。化学兴趣小组为测定其纯度,做了以下实验(杂质溶于水,且不与硝酸银溶液反应),请根据如图所示的实验过程和提供的数据进行计算。

(1)过滤后最终所得固体的质量为 g;
(2)所用硝酸银溶液的溶质质量分数是多少?(写出计算过程)
(3)该化肥是否合格?(写出计算过程,计算结果精确到0.1%)
实验室用质量分数为20.0%的稀硫酸处理含 的废液。向100.0g废液中加入稀硫酸至溶液恰好呈中性,最终得到2.33g沉淀。请计算:
(1)配制490.0g20.0%的稀硫酸需质量分数为98.0%的浓硫酸 g。
(2)废液中 的质量分数。
实验室有部分已变质为碳酸钠的氢氧化钠样品,质量为1.86g。某实验小组将此样品加入水中完全溶解,配成100g溶液,然后向其中缓慢滴加9.8%的稀硫酸,搅拌使气体全部逸出。滴加过程中,相关数据如表:
|
测定次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
滴加稀硫酸总质量/g |
0 |
10 |
20 |
30 |
40 |
|
溶液总质量/g |
100 |
110 |
119.56 |
129.56 |
m |
|
溶液pH |
13.3 |
10.2 |
7.0 |
0.9 |
0.8 |
请回答下列问题:
(1)氢氧化钠(NaOH)由 元素组成。
(2) 中碳原子与氧原子的个数比为 。
(3)第 次测定时,溶液中只有一种溶质。表中m= 。
(4)计算样品中碳酸钠( )的质量分数。(写出计算过程,结果精确到1%)
根据
 反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁 的生铁的质量是多少?
(1)用 克溶质质量分数为 的过氧化氢溶液配制成溶质质量分数为 的过氧化氢溶液,需加水_____克。
(2)取 克某过氧化氢溶液放入锥形瓶中并加入一定量的二氧化锰,用电子秤测其质量,不同时间电子秤的读数如下表所示。试计算该过氧化氢溶液的溶质质量分数(不考虑 逸出,写出计算过程,结果保留到 )。
反应时间/ |
|
|
|
|
|
|
|
锥形瓶+瓶内物质的总质量/ |
|
|
|
|
|
|
|
硫酸铜对过氧化氢( )的分解有催化作用。取8.5%的过氧化氢溶液40g倒入锥形瓶中,向其中加入15%的硫酸铜溶液6.6g,使过氧化氢完全分解,若产生的气体全部逸出,请计算:
(1)过氧化氢的相对分子质量为 。
(2)产生氧气的质量(写出计算过程)。
(3)反应后所得硫酸铜溶液中溶质的质量分数为 。
向氯化铜和盐酸的混合溶液中滴加一定溶质质量分数的氢氧化钡溶液,充分搅拌,加入氢氧化钡溶液的质量与生成沉淀的质量关系如图所示。
请完成下列问题:
(1)a点时,溶液的pH 7。
(2)求所用氢氧化钡溶液中溶质的质量分数。(写出计算过程)

游览活动即将结束,化学精灵请同学们乘坐氢燃料汽车回家。氢气作为燃料具有热值高、无污染的优点,但是制备成本高,储存有难度。若用废旧黄铜( 合金)和稀硫酸为原料制备氢气,测得实验数据如图,请计算:
(1)该废旧黄铜中锌的质量为_____ 。
(2)实验中生成氢气的质量。

我国明代科技著作《天工开物》中有利用炉甘石(主要成分是ZnCO3)火法炼锌的工艺记载,主要反应原理为ZnCO3+2C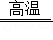 Zn+3CO↑,现用200kg炉甘石与足量碳充分反应,产生CO的质量与加热时间的关系如图所示。
Zn+3CO↑,现用200kg炉甘石与足量碳充分反应,产生CO的质量与加热时间的关系如图所示。
(1)此过程中产生CO的质量是 kg。
(2)列式计算此炉甘石中ZnCO3的质量分数。
夏日鱼塘缺氧,鱼类“浮头”现象多发。养鱼师傅向鱼塘中撒入一种主要成分为过氧化钙( )的白色固体(杂质不与水反应),以解决鱼塘缺氧问题。
(1)影响气体溶解度的外界因素有_____。过氧化钙与水反应生成氢氧化钙和氧气,氢氧化钙对水产养殖颇有益处,列举一项__________。
(2)将 质量分数为 的白色固体 撒入鱼塘,产生氧气(密度为 )的体积是多少?(写出计算过程)
我国科学家在人工合成淀粉领域取得了突破性进展,其基本变化过程为“ 。”淀粉中C、H元素的质量之比为 _____,C的质量分数为_____ (计算结果保留一位小数,下同)。
试题篮
()