【资料阅读】据中国室内装饰协会调查,甲醛污染大部分是由板材产生,家庭装修中使用的夹芯板、地板、家具等都可能释放出甲醛。我国的国家标准检测:“El级板材相当于甲醛释放量为1.5mg/L;E0级板材的甲醛释放量为0.5mg/L。”El级与E0级最大的区别就是甲醛的释放量,E1级比E0级释放甲醛量多五分之一。目前,化学家已能从马铃薯中提取植物胶做板材的黏合剂,有效地减少了甲醛的排放。 试根据上述资料填空。
试根据上述资料填空。
(1)已知甲醛的结构式为 ,则 ,其化学式为 ▲ ,其碳、氢和氧元素的最简质量比为 ▲ ,其含氧元素的质量分数等于 ▲ 。
(2)资料中加点信息有误,实际上E1级比E0级释放甲醛量多了 ▲ ▲倍。
金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于变化。钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择(选填"铜块"、"锌块"、"铅块")。
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为。
②实验室常采用操作进行沉淀分离。
③生产高纯碳酸钙时,选择"220℃恒温干燥"而不选择"灼烧"的原因是。
④高纯氧化钙生产过程中,"干燥"的主要目的是为了防止(用化学方程式表示)。
(3)有机高分子材料"玉米塑料",因其可降解被广泛用来替代一次性泡沫塑料,"玉米塑料"的使用可减少污染。20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用方法区分尼龙和蚕丝。
(7分)下图是对生成氯化钠反应关系的归纳与整理。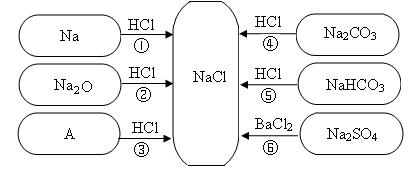
请回答下列问题:
(1)物质A是常见的碱,写出A的化学式:______。
(2)写出反应①的化学方程式:___________________。
(3)说出NaHC03在医疗上的一种用途:______________ 。
(4)反应③、④、⑤、⑥能够进行的原因是_______________。
(5)实验室配制200g 8%的NaCl溶液,需要水的质量是___________g,配制过程中为了加快NaCl的溶解,可以采取的措施是_____________。
A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,G是一种重要建筑材料的主要成分,E是一种金属氧化物,与A反应能生成一种常见的碱。它们之间的转换关系如下图所示:

(1)写出下列物质的化学式:A_、D。
(2)写出反应④的化学方程式。
(3)E在日常生活中用途广泛请写出其中一点。
(4)点燃B、D之前一定要。
(5)B是最清洁的燃料,与其它燃料相比其优点有,但是作为燃料暂时还不能广泛使用你认为的原因是:。
化学来源于生活又服务于生活。下表是生活中常用物质溶液的pH及主要成分化学式:
请结合上表信息回答下列问题:
(1)当你被蚊虫叮咬(释放一种酸性物质)后,为减轻疼痛,可在叮咬处涂 (填序号);
(2)用久的铝壶内有水垢(主要成分为CaCO3),可用 (填序号)少量多次清除。
氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产二水化钙(
)的流程如下。原料石灰石中含有杂质主要是
。
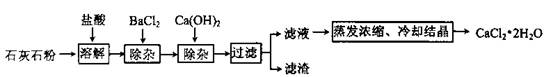
(1)石灰石粉溶解时,
发生反应的化学方程式为。
(2)加入
除去的杂质离子是;加入
除去的杂质离子是。
(3)检验"滤液"酸碱性,如果显碱性,还需加入适量的(填化学式)提高产品纯度。
现有一包固体粉末,可能由
、
、
中的一种或几种组成。为确定其组成,进行了如下图所示的实验(假设实验过程无损耗)。

请回答:
(1)根据实验可以确定白色沉淀是 ;原固体粉末中一定含有,它的可能组成有种。
(2)若实验取固体粉末20
,生成白色沉淀10
,最后得到溶质质量分数为5.85%的
溶液200
(只含一种溶质),则
溶液中溶质的质量是
,固体粉末由(填化学式,下同)组成,其中质量小于10
的是。
硝酸可发生反应:
。据此回答:
(1)反应的基本类型属于反应。
(2)
的化学式为,推断的依据为。
(3)硝酸的保存应注意、。
氯化钙是多用途的干燥剂和建筑防冻剂。实验室里用石灰石和盐酸制备二氧化碳的含酸废液(含有MgCl2、FeCl3等)通过以下途径制得无水氯化钙。
(1)操作I的名称为 ,操作II的名称为 。滤渣 的化学成分有
的化学成分有
。
(2)石灰乳的作用是① ,② ,写出其中1个反应的化学方程式 。
孔雀石主要含Cu2(OH)2CO3〔也可认为是Cu(OH)2·CuCO3〕,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O,步骤如下:
请回答下列问题:
(1)气体E的化学式是 。
(2)由溶液C获得CuSO4·5H2O,需要经过蒸发浓缩、冷却结晶、 和干燥等操作。
(3)写出孔雀石主要成分与稀硫酸反应的化学方程式: 。
构建知识网络是一种重要的学习方法。如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质。请回答下列问题:
(1)C物质的化学式为 。
(2)B物质的一种用途是 。
(3)反应②还需要的一种反应物是 (填化学式)。
(4)写出④反应的化学方程式: 。
(5)反应①导致每年有大量的钢铁锈蚀,为阻止该反应的发生,人们常采用在钢铁表面涂刷油漆或镀上其它金属等方法。这两种方法的共同原理是阻止钢铁与 接触。
(6)市场上出售的补血麦片中常含有微量颗粒细小的还原性铁粉,铁粉与人体胃液中的
发生反应转化为氯化亚铁,起到补血的作用。
甲同学对有关盐的知识进行了以下的整理。

(1)上述盐的排列是依据顺序归纳整理的。
(2)上述盐因组成上相似而具有某些共同的化学性质,如都能与
溶液反应生成硫酸钡沉淀,该反应的化学方程式为(任选其中一种盐即可)。
(3)甲同学通过查阅资料,发现许多反应都有盐类物质生成。他将这些知识间相互关系整理成右图,请将右图补充完整
,
。
(4)乙同学提出可用如图指导进行物质的制备:请写出2个有关硫酸亚铁生成的化学反应方程式。

答:;
。
高纯度的氧化铜可用作颜料、有机合成催化剂等,以下是用粗铜粉氧化法获取高纯度氧化铜的流程图。

回答下列问题:
(1)1:1的硫酸溶液是用1体积98%的浓硫酸与1体积水混合而成,配制该硫酸溶液时,一定要把慢慢注入,并不断搅拌。
(2)写出硫酸与氧化铜反应的化学方程式:。
(3)写出固体
所含的物质:。
(4)洗涤固体
应使用的试剂是。
归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应)。

⑴为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变色;
⑵图中A所表示的物质类别是;
⑶盐酸的性质③决定了盐酸可用于清除铁锈(主要成分
),该反应的化学方程式是;
⑷为了验证性质⑤,可选用的物质是(填一种即可);
⑸镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是(填序号);
| A. | 两种金属的形状 | B. | 盐酸的质量分数 | C. | 反应容器的大小 | D. | 温度 |
医用氯化钙常用于合成药物。以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水和氯化钙(CaCl2·2H2O)的流程如下图所示。
|
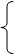
|
滤液…→CaCl2·2H2O
①加盐酸 ② 加Ca(OH)2 ③操作a

 滤渣
滤渣
试题篮
()