(4分) 合成氨工业对国民经济和社会发展具有重要的意义。向2L密闭容器中通入2mol 气体N2和6mol气体H2,在一定条件下发生反应:N2(g)+3H2(g)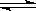 2NH3(g);已知:反应2min达到平衡,此时N2的浓度减少了2/3。
2NH3(g);已知:反应2min达到平衡,此时N2的浓度减少了2/3。
回答下列问题:
⑴反应2min内,用NH3表示该反应的速率是________________;
⑵反应平衡时,N2的转化率为 ;
⑶如果只升高反应温度,其他反应条件不变,平衡时NH3浓度为 1.1mol/L,则该反应的ΔH 0;(填“>”、“<”或“=”)
⑷合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是________(填序号)。
①20 MPa~50 MPa ②500℃的高温 ③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中
⑸如果其他条件不变,将容器的容积变为 1L,进行同样的实验,则与上述反应比较:
反应速率 (填“增大”、“减小”或“不变”),理由是 ;








 粤公网安备 44130202000953号
粤公网安备 44130202000953号