题文
已知A、J、D、E、G是元素周期表中1~36号元素,其原子序数依次增大。A与另外四种元素既不在同一周期,也不在同一主族。J和D同主族,E和G同周期;元素G是周期表中的第7列元素,E的最外层电子数与最内层电子数相同,E跟J可形成离子化合物,其晶胞结构(其中J原子在晶胞内部)如图。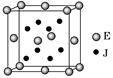
请回答下列问题:
(1)D元素-1价离子的电子排布式为 ;G元素原子的价电子排布式为 。
(2)元素J与氮元素可以形成化合物NJ3,其中N—J键的化学键类型为 ,根据价层电子对互斥理论可以判断NJ3的空间构型为 ,NJ3分子中N原子的杂化方式为 杂化。
(3)A、J形成的化合物AJ的相对分子质量比A、D形成的化合物AD的相对分子质量小,但AJ的沸点比AD高,其原因是 。
(4)从晶胞图可以得出:E与J形成的离子化合物的化学式为 。
(5)含有E元素的化合物焰色反应为 色,焰色反应的原理是 。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号