(12分)化学实验是研究物质性质的基础。
(1)下列有关实验操作或测量数据不合理的是______(填序号)。
A.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
B.用干燥的pH试纸测定浓硫酸的pH
C.用规格为20 mL的量筒,量取16.8 mL的Na2CO3溶液
D.用已知浓度盐酸滴定未知浓度氨水,用酚酞做指示剂。
(2) 某废水样品中含有一定量的Na+、CO 、SO
、SO ,某研究小组欲测定其中SO
,某研究小组欲测定其中SO 的浓度。
的浓度。
实验方案:
ⅰ.用烧杯盛取废水适量,加少量活性炭,除去废水中的杂质;过滤,取滤液;
ⅱ.精确量取20.00 mL过滤后废水试样,选择使用紫色的0.1 mol·L-1 KMnO4(H2SO4酸化)溶液进行滴定;
ⅲ.记录数据,消耗KMnO4(H2SO4酸化)溶液体积Vml,计算。
①下列滴定方式中,最合理的是(夹持部分略去)________(填字母序号)。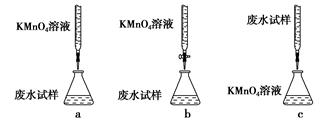
②达到滴定终点时现象是: 。SO 的浓度的表达式为: 。
的浓度的表达式为: 。
(3) 已知反应: BeCl2+Na2BeO2+2H2O =" 2" NaCl+2Be(OH)2 ↓能进行完全, 据此判断下列叙述正确的是:
A、BeCl2溶液的 pH<7, 将其蒸干灼烧后得到的残留物为 Be(OH)2
B、Na2BeO2溶液的 pH>7, 将其蒸干灼烧后得到的残留物为 BeO
C、Be(OH)2既能溶解于盐酸, 又能溶解于 NaOH 溶液
D、Na2BeO2溶液中守恒关系有:C(Na+)+ C(H+)= 2c(BeO22-)+C(OH-)+C(H2BeO2)
E 、Li 、 Be 、 B 三种元素的第一电离能异常小的 B 元素。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号