常温下,向Na2CO3溶液中逐滴滴入0.1mol/L盐酸,溶液的pH随着滴入盐酸溶液体积变化曲线如下图,则下列说法正确的是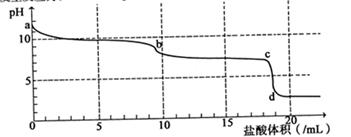
| A.a点时溶液pH=11.5,原因是:CO32-+H2O=HCO3-+OH- |
| B.a-b段发生反应为:CO32-+2H+=CO2↑+H2O |
| C.b-c段发生反应为:HCO3-+H+=CO2↑+H2O |
| D.c-d段发生反应为:H++OH-=H2O |
常温下,向Na2CO3溶液中逐滴滴入0.1mol/L盐酸,溶液的pH随着滴入盐酸溶液体积变化曲线如下图,则下列说法正确的是
| A.a点时溶液pH=11.5,原因是:CO32-+H2O=HCO3-+OH- |
| B.a-b段发生反应为:CO32-+2H+=CO2↑+H2O |
| C.b-c段发生反应为:HCO3-+H+=CO2↑+H2O |
| D.c-d段发生反应为:H++OH-=H2O |
试题篮
()