为研究草酸亚铁晶体(FeC2O4·2H2O,相对分子质量是180)分解的产物,在实验室里称取一定量的草酸亚铁晶体,利用下列装置进行实验。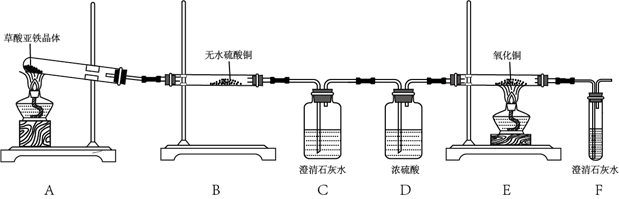
①实验过程中观察到B中白色无水CuSO4变色蓝色,C、F中澄清石灰水变浑浊;则E中现象是____(填实验现象)。分解产物中有CO气体,还有______________。
②若该实验过程中E装置内有6.4g铜生成,计算有多少物质的量的氧化铜参加了反应?(写出反应的化学方程式,列出计算步骤!)____________
写出方程式:____________
计算步骤:____________
③为验证CO的性质,收集装置D后的气体于集气瓶中,将点燃的木条伸入集气瓶中(如下图),在此过程中的实验现象是_____________(选填编号)。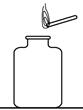
A.木条熄灭 B.木条继续燃烧
C.瓶口产生淡蓝色火苗 D.发生爆炸
④进行上述实验时,先点燃A处的酒精灯,一段时间后再点燃E处的酒精灯,原因是____________。
⑤若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产生物中有CO,则需在C和D装置之间增加如下图所示的洗气瓶: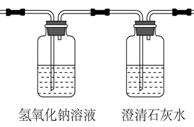
其中氢氧化钠溶液中发生的反应方程式是:___________________________;
澄清石灰水起到的作用是:___________________________________________________。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号