[化学——选修3:物质结构与性质]X、Y、Z、W是原子序数依次增大的前四周期元素。X的三个能级中排布的电子数相等;Y基态原子的未成对电子数与能级数相等;Z位于X的下两个周期,其电离能数据分别是:I1 = 419kJ·mol-1,I2 =" 3051" kJ·mol-1,I3 =" 4411" kJ·mol-1;W3+的核外电子排布式是[Ar]3d5。回答下列问题:
(1)X、Y、Z三种元素电负性由大到小的顺序为_________。
(2)X的某种氧化物与Y2互为等电子体,写出该氧化物的结构简式_________,该氧化物所含的化学键类型是_________。
(3)YH4+的空间构型是_________ 。X原子的杂化方式均为sp2、相对分子质量最小的X的氢化物分子式为_________。
(4)四种元素可形成化合物Z4[W(XY)n],W原子的最外层电子数和配体形成配位键时提供的电子数之和为14,则 n ="_________" 。
(5)下图____ (填“A”、“B”或“C”)表示的是Z晶体中微粒的堆积方式。若Z晶体中一个晶胞的边长为a pm,则Z晶体的密度为____________(写出含a的表达式,用NA表示阿伏伽德罗常数)。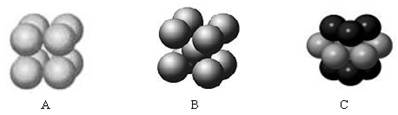








 粤公网安备 44130202000953号
粤公网安备 44130202000953号