工业上,可以由下列反应合成三聚氰胺:
CaO+3C CaC2+CO↑;CaC2+N2
CaC2+CO↑;CaC2+N2 CaCN2+C;CaCN2+2H2O=NH2CN+Ca(OH)2
CaCN2+C;CaCN2+2H2O=NH2CN+Ca(OH)2
NH2CN与水反应生成尿素[CO(NH2)2],再由尿素合成三聚氰胺。
(1)写出与Ca在同一周期的Cu原子的基态电子排布式 。
(2)写出CaC2中阴离子C22-的一种等电子体的化学式 。
(3)1mol 尿素分子[CO(NH2)2]中含有的π键与σ键的数目之比为 。
(4)三聚氰胺俗称“蛋白精”,其结构为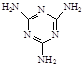 。其中氮原子的杂化方式有 。
。其中氮原子的杂化方式有 。
(5)CaO晶胞如下图所示,CaO晶体中与O2-距离最近的O2-的个数为 。CaO晶体的熔点比NaCl晶体的熔点高的主要原因是 。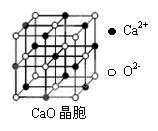








 粤公网安备 44130202000953号
粤公网安备 44130202000953号