海水中含有丰富的镁资源。锂(Li)与镁元素性质相似。
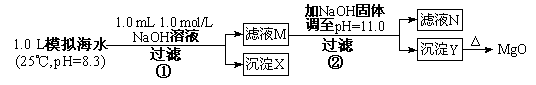
(1)某同学设计了从模拟海水中制备MgO的实验方案:
| 模拟海水中的 离子浓度(mol/L) |
Na+ |
Mg2+[来 |
Ca2+ |
Cl― |
HCO3―[来源 |
| 0.439 |
0.050 |
0.011 |
0.560 |
0.001 |
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp [Mg(OH)2]=5.61×10-12
请回答:沉淀物X为 (写化学式);滤液N中存在的金属阳离子为 ;
步骤②中若改为加入 4.2 gNaOH固体,沉淀物Y为 (写化学式)。
(2)物质的量为0.10 mol的锂在只含有N2和O2混合气体的容器中燃烧,反应后容器内固体物质的质量m克,m的取值范围是 ;
(3)锂电池是新一代高能电池,目前已研究成功多种锂电池。某离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为LiCoO2+C6 CoO2+LiC6,则放电时电池的正极反应为 ;
CoO2+LiC6,则放电时电池的正极反应为 ;
(4)为了回收废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量AI、Fe等)可通过下列实验方法回收钴、锂。
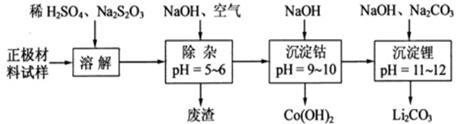
①在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中的化学反应方程式为 。
②调整PH=5-6的目的是 。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号