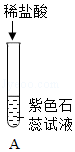
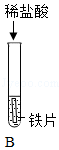
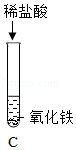
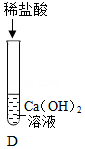
为探究酸的化学性质,某化学小组利用盐酸进行了如下实验操作:
实验 |
|
|
|
|
|
请回答:
(1)写出E中反应的化学方程式 。
(2)将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行如下探究:
[提出问题]滤液中溶质的成分是什么?
[作出猜想]
猜想一:NaCl
猜想二:NaCl和CaCl2
猜想三:NaCl、CaCl2和Na2CO3
猜想四: 。
[进行讨论]经过讨论,同学们一致认为猜想 是错误的。
[设计实验]请完成实验报告。
实验步骤 |
实验现象 |
实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液 |
无明显现象 |
猜想二不成立 |
取少量滤液于试管中,滴加氯化钡溶液 |
|
猜想四成立 |
[反思拓展]在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑 。







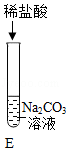

 粤公网安备 44130202000953号
粤公网安备 44130202000953号