阅读下面科普短文。
氨(NH3)常用来制化肥和硝酸,但是科学家们发现它还是一种很有前景的燃料。
现有的化石燃料燃烧时,都会产生温室气体CO2,而氨燃烧时生成N2和H2O两种对环境友好的产物。氨价格低、制造技术成熟,便于普及使用。传统的工业合成氨是将氮气和氢气在20~50MPa的高压和500℃的高温条件下,用铁作催化剂合成的。
氨很容易液化,将氨常温下加压到1MPa,或者常压下温度降到-33℃,均可将其液化。而为了获得含有相同能量的液态氢(H2),常温下需要136MPa的压力来压缩它,显然超出了车载燃料储存的压力极限。
氨虽然有毒, 但氨具有强烈的刺激性气味,一旦发生泄漏,达到人们觉察到时浓度的1000倍才会致命,因此很容易被发现并及时补救。氨比空气轻, 泄漏后扩散快, 不会聚积。泄漏在大气中的氨还可以参与自然循环,随雨雪移动后,与其他物质反应或被植物吸收。
依据文章内容,回答下列问题。
(1)化石燃料都会生成CO2的原因是___________________。
(2)文中提到氨的物理性质有 (答出两点)。
(3)从阅读材料中可以看出,将气体液化的途径有_________________。
(4)请写出氨燃烧生成N2和H2O的化学方程式___________________。
(5)德国化学家格哈德·埃特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程。下图为该过程的微观示意图(图中 表示氮原子,
表示氮原子, 表示氢原子,
表示氢原子, 表示催化剂)。符合上述反应过程的顺序是 (填字母序号)。
表示催化剂)。符合上述反应过程的顺序是 (填字母序号)。

| A.⑤④①③② | B.④⑤①②③ | C.④⑤①③② | D.⑤④①②③ |
金属的利用非常广泛。
(1)地壳中含量最高的金属元素是 。
(2)下列物品中,利用金属导电性的是 (填字母序号)。

A.黄金饰品 B.铁锅 C.铜导线
(3)中国是自行车大国。钢材是使用在自行车上最久的车架材质,钢的缺点是易生锈,生锈的原因是铁与 反应的结果。
海水淡化可解决淡水资源缺乏的问题。右图是海水淡化的一种装置。
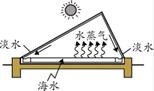
(1)请从能源角度指出其优点: (答出一点即可)。
(2)检验所获取的淡水是否为软水,常用的试剂是 。
(3)该过程中主要发生的是 (填“物理”或“化学”)变化。
下列物质的用途与性质对应关系错误的是
| 选项 |
A |
B |
C |
D |
| 用 途 |
 |
 |
 |
 |
| 干冰用于人工降雨 |
活性炭作口罩滤芯 |
碳棒(含石墨)作电极 |
蜡烛在空气中燃烧 |
|
| 性质 |
干冰升华后的气体 密度大于空气 |
活性炭吸附性 |
石墨导电性 |
氧气助燃性 |
空气也是一种重要的资源。
(1)利用膜分离法可制得富氧空气。当空气通过膜分离装置时,由于氧分子能透过膜而氮分子不能透过膜,就把空气中的氧气和氮气分离开了。分离过程中发生了 变化。
(2)利用膜分离获得的富氧空气可用于 (填一种用途)。
下表中所描述的变化与右图相符合的是

| |
化学变化 |
Y轴 |
a |
b |
| A |
等质量的高锰酸钾和水在不同条件下分解 |
氧气质量 |
高锰酸钾 |
水 |
| B |
等质量、等浓度的双氧水在不同条件下反应 |
氧气质量 |
加催化剂 |
加热 |
| C |
等质量的镁片和铁片分别与足量的稀硫酸反应 |
氢气质量 |
镁 |
铁 |
| D |
等质量的二氧化碳和生石灰分别与等量的水反应 |
温度 |
二氧化碳 |
生石灰 |
下列说法中,与化学变化中遵循的质量守恒定律不相符合的是
| A.水结冰后,质量保持不变 |
| B.铜粉在空气中加热后,质量增大 |
| C.蜡烛在空气中燃烧后,质量减小 |
| D.1.2 g碳与3.2 g氧气完全反应,生成4.4 g二氧化碳 |
下列食品、调味品的制作过程中,主要发生物理变化的是
| A.水果榨果汁 | B.黄豆酿酱油 | C.糯米酿甜酒 | D.鲜奶制酸奶 |
合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主要流程如下:
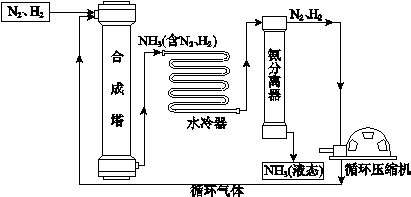
(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是 。
(2)生产过程中可循环使用的物质是 。
(3)根据表中的数据回答问题。
| 物质 |
H2 |
N2 |
O2 |
NH3 |
| 沸点/℃(1.01×105 Pa) |
–252 |
–195.8 |
–183 |
–33.35 |
在1.01×105 Pa时,欲将NH3与N2、H2分离,适宜的方法是 。
下列物质的用途中,利用其化学性质的是
| A.液氮用于冷冻 | B.天然气用作燃料 |
| C.石墨用作电极 | D.稀有气体用作电光源 |
在“宏观”、“微观”、“符号”三者之间建立联系是化学学科特有的思维方式。
(1)①FeO名称:____ ;
②Mg2+中2表示的意义: ;
③2Hg表示的意义:____ 。
(2)写出实验室制取二氧化碳气体的化学方程式:____________________________。
(3)酒精检测仪中的反应原理:C2H5OH +4X +6H2SO4=2Cr2(SO4)3 +2CO2↑+9H2O,推测X的化学式为 。
(4)已知:甲+乙_丙+丁。
①若反应物分别为单质和化合物,写出一个符合条件的化学方程式.
②若反应的微观示意图如下,写出化学方程式:______________。

下列有关物质的描述属于化学性质的是
| A.汽油易挥发 | B.高梁能酿酒 |
| C.铁熔点为1535℃ | D.铝导电性好 |
阅读下面的短文,回答问题
认识二恶英
1976年7月意大利塞维索一家化工厂爆炸,剧毒化学品二恶英扩散,使3.7万人中毒受害。事隔多年后,当地居民的畸形儿出生率大为增加。1999年震惊世界的二恶英公害事件发生在比利时,鸡肉、牛奶二恶英被污染,损失超过10亿欧元,导致了比利时政府内阁的集体下台。
二恶英中以2,3,7,8-四氯-二苯并对二恶英(2,3,7,8-TCDD)的毒性最强,它的化学式是C12H4Cl4O2,①熔点较高,为302~305℃;②极难溶于水,可以溶于大部分有机溶剂;③二恶英非常稳定,与酸碱不起反应,不易燃烧;④在500℃开始分解,800℃时,21秒内完全分解,它在一般环境下,氧化和水分解的速率非常低,在土壤内残留时间为10年;⑤是无色无味的固体物质;⑥有毒,其毒性是氰化物的130倍、砒霜的900倍,有“世纪之毒”之称。国际癌症研究中心已将其列为人类一级致癌物。
二恶英的发生源主要有两个,一是在制造含氯杀虫剂、除草剂、木材防腐剂、落叶剂(美军曾用于越战)等产品的过程中派生;二最主要的来源(占90%)是城市和工业垃圾焚烧,在对聚氯乙烯等含氯塑料的焚烧过程中,焚烧温度低于800℃会不完全燃烧,极易生成二恶英。二恶英随烟雾扩散到大气中,通过呼吸进入人体的是极小部分,更多的则是通过食品被人体吸收。以鱼类为例,二恶英粒子随雨落到江河湖海,被水中的浮游生物吞食,浮游生物被小鱼吃掉,小鱼又被大鱼吃掉,二恶英在食物链全程中慢慢积淀浓缩,等聚在大鱼体内的浓度已是水中的3000多倍了,而处于食物链顶峰上的人类体内将会聚集更多的二恶英。可怕的是一旦摄入二恶英就很难排出体外,积累到一定程度,它就引起一系列严重疾病。
2001年国家环保总局组织的抽样调查显示,所抽取的垃圾焚烧厂烟气二恶英超标率为57.1%,有的落后垃圾焚烧设施二恶英超标99倍以上。因此,环保部门号召对垃圾进行分类收集和处理,控制无组织的垃圾焚烧,通过采用新的焚烧技术,提高燃烧温度(1200℃以上),降低二恶英类的排放量。
请回答:
(1)2,3,7,8-四氯-二苯并对二恶英(2,3,7,8-TCDD)的化学性质包括 ,物理性质包括 (以上两空填第二自然段的序号)。
(2)2,3,7,8-四氯-二苯并对二恶英中含 种元素,各元素的质量比为 。
(3)作为一名具备一定科学素养的中学生,看到学校、村子或垃圾箱等处有人随意焚烧塑料垃圾时,你应该如何做?
下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是
A.拉瓦锡测定空气中氧气的含量 4P+5O2 P2O5化合反应 P2O5化合反应 |
B.比较铜和银的金属活动性 Cu + 2AgNO3 Cu(NO3)2 +2Ag置换反应 Cu(NO3)2 +2Ag置换反应 |
C.用硫酸除铁锈 Fe2O3 +2H2SO4 2FeSO4 +3H2O置换反应 2FeSO4 +3H2O置换反应 |
D.煅烧石灰石制生石灰 CaCO3 CaO + CO2↑分解反应 CaO + CO2↑分解反应 |
试题篮
()