已知胰岛素含硫的质量分数为3.4%,相对分子质量为5734,则每个胰岛素分子中所含的硫原子数为
| A.2 | B.4 | C.6 | D.8 |
只含碳、氢、氧的有机物,为便于研究其燃烧时,生成物与所需氧气的量的关系,可用通式(CxHy)m(H2O)n或(CxOy)m(H2O)n表示它们。(m、n、x、y 均为正整数)
例如:CH3OH、C2H5OH、C3H7OH等物质可用通式(CH2)m(H2O)n表示,其m分别为1,2,
3,n均为1。它们燃烧时所需的氧气和生成的二氧化碳的体积比均为3∶2。
(1)现有一类只含C、H、O的有机物。它们燃烧时所需消耗的氧气和生成的二氧化碳的体积比为5∶4(相同状况),按照上述要求,该类化合物的通式可表示为
(2)写出这类化合物分子量最小的物质的结构简式 。
(3)写出这类化合物中生成CO2与H2O的物质的量之比为1∶1,且能发生水解反应的物质的分子式 ,该物质能发生水解的同分异构体有 种。
(4)若某一类有机物可用通式(CxOy)m(H2O)n表示,则在相同的条件下,该类化合物完全燃烧时消耗的氧气体积为V1和生成的CO2体积为V2,则V1、V2必须满足的条件是
。
(5)现有一种有机物,它完全燃烧时,消耗氧气与生成CO2的体积比为3∶4,它具有两个羧基,其余的碳原子与相同的原子或原子团结合,取0.2625g该化合物恰好能与2500ml
0.10 00mol·L-1的NaOH完全中和,由此可知该化合物的分子式应是
结构简式为 。
Ⅰ.下图中A、B、C分别是三种有机物的结构模型:
请回答下列问题:
(1)A及其同系物的分子式中的碳原子数用n表示。当n=_______时,烷烃开始出现同分异构体。B模型是有机物的________模型。
(2)结构简式为 的有机物中,分子中最多有 个原子共面。
的有机物中,分子中最多有 个原子共面。
(3)等质量的A、B、C三种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状况下)最大的是________(填分子式)。
Ⅱ.在有机物分子中,不同氢原子的核磁共振氢谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是________。
A.CH3COOH B.C(CH3)4 C.CH3COOCH3 D.CH3OH
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如下图所示,则A的结构简式为________。
(3)用核磁共振氢谱的方法来研究C2H6O的结构,简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是_______________________ _ 。
5.8 g某有机物Q完全燃烧可产生13.2 g CO2和0.3 mol H2O。已知Q蒸气对氢气的相对密度是29;Q能发生酯化反应,分子中不含甲基,为链状结构。请通过计算确定Q的稳定结构的结构简式(烯醇式:C=C—OH不稳定)。
某有机物X含C、H、O三种元素,现已知下列条件:
①碳的质量分数;②氢的质量分数;③蒸汽的体积(已折算成标准状况下的体积);
④X对氢气的相对密度;⑤X的质量;⑥X的沸点,
确定X的分子式所需要的最少条件是
A.①②⑥ B.①③⑤ C.①②④ D.①②③④⑤
2012年2月20日《南方日报》A12版报道了如下几种饮料添加剂:对羟基苯甲酸甲酯、苯甲酸钠、塑化剂等,请回答以下相关问题:
(1)对羟基苯甲酸甲酯的分子式为________。请写出对羟基苯甲酸甲酯符合下列所有条件的任意一种同分异构体________。
A.有醛基 B.有苯环 C.苯环上氢只有一种
(2)苯甲酸钠________(填“难”或“易”)溶于水,其水溶液显________(选填“酸”、“碱”或“中”)性,理由是____________________________________________________________(用离子方程式表示)。
(3)邻苯二甲酸二丁酯是塑化剂之一,它的另外两种性质基本相同的同分异构体是______________________________________________________________________
为测定某有机物的结构,用核磁共振仪处理后得到下图所示的核磁共振氢谱,则该有机物可能是
| A.C2H5OH | B. |
C. |
D. |
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。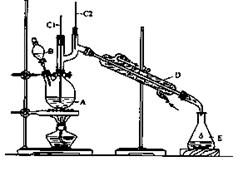
发生的反应如下:
CH3CH2CH2CH2OH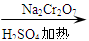 CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| |
沸点/。c |
密度/(g·cm-3) |
水中溶解性 |
| 正丁醇 |
11.72 |
0.8109 |
微溶 |
| 正丁醛 |
75.7 |
0.8017 |
微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,并说明理由 。
(2)加入沸石的作用是 。若加热后发现未加沸石,应采取的正确方法是 。
(3)上述装置图中,B仪器的名称是 ,D仪器的名称是 。
(4)分液漏斗使用前必须进行的操作是 (填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”)
(6)反应温度应保持在90—95℃,其原因是 。
(7)本实验中,正丁醛的产率为 %。
经分析,某芳香族化合物A含有C、H、O的质量分数分别为77.8%、7.4%、14.8%,该有机物相对分子质量为108。
(1)通过计算,写出该有机物的分子式。
(2)如果该有机物遇FeCl3溶液显紫色,写出满足要求的所有有机化合物分子的结构简式。
有机物A是一种纯净的无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A物质 18.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为_ _ |
(2)A的核磁共振氢谱如图: |
(2)A中含有_____种氢原子 |
| (3)另取A 18.0 g与足量的NaHCO3粉末反应,生成0.2 mol CO2,若与足量钠反应则生成0.2 mol H2。 |
(3)写出一个A分子中所含官能团的名称和数量___ |
| (4)将此18.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者依次增重10.8 g和26.4 g。 |
(4)A的分子式为____ |
| (5)综上所述A的结构简式____ ___。 |
下列化合物的核磁共振氢谱中出现三个峰的是
| A.2,2,3,3四甲基丁烷 | B.2,3,4三甲基戊烷 |
| C.3,4二甲基己烷 | D.2,5二甲基己烷 |
相对分子质量不超过100的有机物A能与碳酸钠反应产生无色气体;1 mol A还可以使含溴160 g 的四氯化碳溶液恰好褪为无色;A完全燃烧只生成CO2和H2O;经分析其含氧元素的质量分数为37.21%。
(1)试写出A中含有的官能团的名称:_______________________。
(2)经核磁共振检测发现A的图谱如下: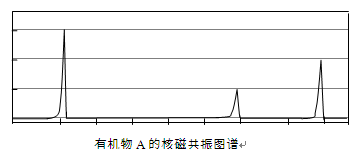
①写出A的结构简式: 。
② A具有下列性质中的(选填字母)_____________:
a.能使酸性高锰酸钾溶液褪色 b.能使溴水褪色
c.能与乙醇和浓硫酸混合液发生反应 d.能与金属钠反应
③ A在一定条件下可以发生聚合反应生成高分子化合物,写出反应的方程式:
(3)相对分子质量与A相同的某烃C有多种同分异构体,请写出其中核磁共振氢谱中峰面
积比最大的C的结构简式: 。
(1)某有机物A的质量为9.2克,完全燃烧后生成0.4mol二氧化碳和10.8克水,且此有机物的蒸气的相对密度是相同状况下氢气的23倍,求:
①此有机物的分子式为
②写出该有机物可能的结构简式
(2)某烃B的相对分子质量为84。回答下列问题:
①下列物质与B以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号) 。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
②若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种, 则B的结构简式为 。
③若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的结构简式为 。
(3)C1(一碳化学)是以含一个碳原子的化合物如:甲烷(CH4)、合成气(CO和H2)、CO2、CH3OH、HCHO等为初始反应物,反应合成一系列重要的化工原料和燃料的化学。
①CO与H2按一定比例可合成乙二醇(C2H6O2),则n(CO)/n(H2)= 。
②汽油平均组成用CmHn表示,则合成汽油应控制n(CO)/n(H2)= 。(用m 、 n表示)
下列说法正确的是
| A.某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则有机物的组成为一定CnH2n |
| B.相同物质的量的烃,完全燃烧,生成的CO2越多,说明烃中的碳的百分含量越大 |
| C.气态烃CxHy在O2充分燃烧,反应前后气体体积不变(温度>100℃),则y=4 |
| D.相同质量的烃,完全燃烧,消耗O2越多,烃中碳的百分含量越高 |
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应方程式和实验装置如下: 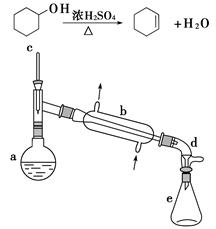
可能用到的有关数据如下:
| |
相对分 子质量 |
密度/ (g·cm-3) |
沸点/℃ |
溶解性 |
| 环己醇 |
100 |
0.961 8 |
161 |
微溶于水 |
| 环己烯 |
82 |
0.810 2 |
83 |
难溶于水 |
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5% 碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
(1)装置b的名称是__________。
(2)加入碎瓷片的作用是________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案序号)。
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为______________。
(4)分液漏斗在使用前必须清洗干净并______。在本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口倒出”)。
(5)分离提纯过程中加入无水氯化钙的目的是__________________。
(6)在环已烯粗产物蒸馏过程中,不可能用到的仪器有______(填正确答案序号)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
试题篮
()