X、Y、Z、T、W五种元素的性质或原子结构如下表:
| 元素 |
元素性质或原子结构 |
| X |
原子的最外层电子数是次外层电子数的2倍 |
| Y |
常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z |
基态原子最外层电子排布式为(n+1)sn(n+1)pn+2 |
| T |
与Z同周期,元素最高价是+7价 |
| W |
原子序数为Y、T元素之和,不锈钢中含有该元素 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是_______;W元素基态原子电子排布式为________________________。
(2)元素Z与元素T相比,非金属性较强的是_______(用元素符号表示),下列表述中能证明这一事实的是______________。
A.常温下Z的单质和T的单质状态不同
B.T的氢化物比Z的氢化物稳定
C.一定条件下Z和T的单质都能与氢氧化钠溶液反应
D.T的电负性比Z大
(3)常见溶剂XZ2的分子中,含有的 键与π键个数比为_______,它所形成的晶体类型为_______;Y的常见氢化物易液化的主要原因是______________
键与π键个数比为_______,它所形成的晶体类型为_______;Y的常见氢化物易液化的主要原因是______________
(4)①自然界常见的X元素含氧酸的钙盐和适量T的氢化物溶液反应时,每产生4. 4g 气体(不考虑气体溶解)放热a kJ,则该反应的热化学方程式为______________。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得PH变化曲线如下图所示: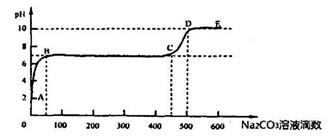
请用离子方程式表示BC段、CD段发生的反应:
BC段:__________________________________________;
CD段:__________________________________________。
Q、R、X、Y、Z(Q、R、X、Y、Z分别代表元素符号)五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn;
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。请回答下列问题:
(1)Z2+的核外电子排布式是 ;在[Z(NH3)4]2+离子中,Z2+的空间轨道接受NH3分子提供的 形成配位键。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,财甲、乙的稳定性大小为 > ,甲、乙的沸点大小为 < (均用相应的化学式表示)。
(3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 < < (用元素符号作答);Q的一种氢化物相对分子质量为26,其中分子中的  键与π键的键数之比为 。
键与π键的键数之比为 。
(4)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 。
下表为部分短周期元素化合价及其相应原子半径的数据。请回答下列问题: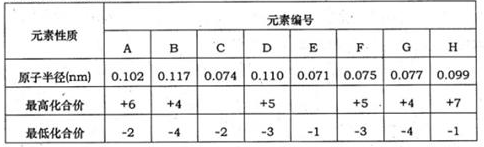
(1)元素G在周期中的位置是 ;元素F所形成的常见单质的电子式为 。
(2)A、B、C、E的氢化物稳定性顺序是 。(用化学式回答)
(3)分子组成为ACH2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是 。
(4)请写出B的单质的一种重要用途 ;工业上制取该单质的原理反应为 。
(5)请设计一个实验方案,使铜和A的最高价氧化物对应的水化物的稀溶液反应,得到蓝色溶液和氢气。请在方框内绘出该实验方案原理装置示意图。
A、B、C、D为原子序数依次增大的四种短周期元素,其性质或结构信息如下表:
试回答以下问题
(1)B在周期表中的位置是 。B的氢化物与E的氢化物比较,沸点较高的是 (填化学式),在水中溶解度较大的是 (填化学式)
(2)写出D3B与甲反应所得溶液呈 (填“酸性”、“碱性”或“中性”),原因是(用化学方程式表示) 。
(3)写出丙的电子式为 。说明丙的水溶液在放置过程中其酸性会增强的原因(用离子方程式表示) 。
(4)由A、B、C、D四种元素中的三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈碱性。可用来鉴别丁和氯化钠的试剂有 。
A.氢碘酸和淀粉的混合液
B.AgNO3溶液
C.甲基橙试剂
D.稀硫酸
(5)将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成深绿色溶液,写出该反应的离子方程式 。
X、Y、Z、W四种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中Y与Z为同一周期,X与W为同一主族,Z元素的外围电子排布为nsnnp2n,W在空气中燃烧可以得到淡黄色固体。又知四种元素分别形成的常见单质在常温常压下有三种是气体,一种是固体。请回答下列问题:
(1)W在元素周期表中的位置是 ;基态时Y的电子排布式是___。
(2)比较元素Y和Z的第一电离能:Y Z(填“大于”、“小于”或“不确定”),将YX3通入溴水中可发生反应,生成Y的单质和一种盐M,Y的单质中的σ键和π键个数比为 ,盐M的晶体类型是 。
(3)由W和Y组成的化合物易水解,其水解的化学方程式是 ;
(4)已知Y2X4和过氧化氢混合可作火箭推进剂。12.8g液态Y2X4与足量过氧化氢反应生成Y的单质和气态水,放出256.65kJ的热量:
2H2O2(l) = O2(g)+2H2O(l) ΔH=-196.4KJ/mol
H2O(l) = H2O(g) ΔH=+44KJ/mol
写出液态Y2X4和氧气反应生成Y的单质和液态X2Z的热化学方程式 。
已知X、Y、Z、M、W、R是前四周期中的六种元素。X元素原子形成的离子是一个质子,Y原子的价电子构型为2s22p2,Z的单质在常温下是无色气体且Z原子的单电子个数是同周期元素原子中最多的。
(1) 24R原子最外层的电子排布图是 ,ZO3-的空间构型是 ;
(2) Z、M、W原子序数依次增大,三种元素的第一电离能由大到小的顺序是 ;Y、Z、W三种元素的电负性由大到小的顺序是 。(填元素符号)
(3) Ne与Wn-的电子数相同,W所在族的各元素的氢化物的水溶液均显酸性,则该族元素的氢化物中沸点最低的是 。(填化学式)
(4)ZX4W在物质中,各种粒子间的相互作用力包括 。(填字母编号)
| A.非极性共价键 | B.极性共价键 | C.配位键 | D.离子键 E.氢键 |
(1)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小。D能分别与A、B、C形成电子总数相等的多原子分子M、N、W,且在M、N、W分子中,A、B、C原子都采取sp3杂化。
①A、B、C的第一电离能由小到大的顺序为_____ (用元素符号表示)。A22-与C22+互为等电子体,C22+的电子式__________
②N的沸点比其同族相邻氢化物沸点高的主要原因是_____。W分子的空间构型的名称是_________
(2)E、F、G三元素的原子序数依次增大,它们原子的最外层电子排布均为4s1。
①F元素基态原子电子排布式为_____
②E元素单质的晶体堆积模型为_____(填字母)
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
③向G的硫酸盐溶液中通入过量N气体,可生成[G(N)4]2+不考虑空间构型,[G(N)4]2+
的结构可用示意图表示为_____ (用元素符号表示)。
X、Y、Z、Q、T五种元素位于前四周期,且原子序数依次增大。X、Y的单质在常温常压下呈气态,X 形成的单质分子中无孤电子对,Y的基态原子中p能级上有两个未成对电子,Z原子的半径在同周期主族元素中最大, Q的氧化物是形成酸雨的一种主要物质,T2+所含有的电子数等于Z和Q原子的电子数之和。
(1)Q元素位于元素周期表第 周期 族,T2+的电子排布式为 。
(2)Y元素和Q元素分别形成的组成相似的氢化物中,沸点较高的是 (写化学式),原因是
用惰性电极电解X、Y、Z三种元素形成的化合物水溶液,其阳极的电极反应式为 。
(3)Z与Q形成的化合物的水溶液呈 填“酸性”、“中性”或“碱性”),原因
是 (用离子方程式表示)。
(4)已知在25℃、101325Pa时:
2T(s)+Q(s)=T2Q(s) △H=-79.5KJ/mol
Q(s)+Y2(g)=QY2(g) △H=-296.6KJ/mol
根据上述反应,请写出T2Q与Y2反应生成T与 QY2的热化学方程式 。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式)。
(2)Q的元素符号是 ,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(3)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主
族,可形成离子化合物ZX,Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),
非金属气态氢化物还原性最强的是 (写化学式)。
(3)X2M的燃烧热△H=-a kJ·mol-1,写出X2M燃烧反应的热化学方程式: 。
(4)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。
X、Y、Z均为短周期元素,X元素的气态氢化物的水溶液滴入无色酚酞变红,Y元素的最外层电子数是次外层电子数的2倍,Z元素是短周期元素中原子半径最大的元素(He、Ne、Ar除外)。
(1)写出X的元素符号 ,其原子结构示意图为 。
(2)元素Y的最简单氢化物的化学式 。
(3)Z元素原子的质子数为 ,Z元素的最高价氧化物对应的水化物的电子
式为 。
(4)X元素最高价氧化物对应的水化物与氧化铝反应的离子方程式为 。
(5)Y元素的最高价氧化物和Z元素的过氧化物发生氧化还原反应的化学方程式为 。
五种短周期元素、
、
、
、
的原子序数依次增大,
和
同族,
和
同族,
离子和
离子具有相同的电子层结构。
和
、
、
均能形成共价型化合物。
和
形成的化合物在水中呈碱性,
和
形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是,非金属性最强的是(填元素符号);
(2)由和
、
、
所形成的共价型化合物中,热稳定性最差的是(用化学式表示);
(3)和
形成的化合物与
和
形成的化合物反应,产物的化学式为,其中存在的化学键类型为;
(4)最高价氧化物的水化物的化学式为;
(5)单质在充足的单质
中燃烧,反应的化学方程式为;
在不充足的
中燃烧,生成的主要产物的化学式为;
(6)单质与水反应的离子方程式为。
、
、
、
是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 |
相 关 信 息 |
(1)位于元素周期表第周期第族;
的原子半径比X的(填"大"或"小")。
(2)的第一电离能比
的(填"大"或"小");
由固态变为气态所需克服的微粒间作用力是;氢元素、
、
的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称。
(3)振荡下,向单质与盐酸反应后的无色溶液中滴加
溶液直至过量,能观察到的现象是;
的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是。
(4)在25℃、101下,已知13.5
的
固体单质在
气体中完全燃烧后恢复至原状态,放热419
,该反应的热化学方程式是。
、
和
均为短周期元素,原子序数依次增大,
的单质为密度最小的气体,
原子最外层电子数是其周期数的三倍,
与
原子最处层电子数相同。回答下列问题:
(1)、
和
的元素符号分别为 、、。
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有、。
(3)和
组成的化合物中,既含有极性共价键又含有非极性共价键的是。
此化合物在酸性条件下与高锰酸钾反应的离子方程式为;此化合物还可将碱性工业废水中的氧化为碳酸盐和氨,相应的离子方程式为。
B、C、D、E均是短周期元素。B元素原子最外层上的电子数为内层电子总数的2倍。B元素原子和C元素原子最外层电子数之差为2。C和D形成的化合物进行焰色反应火焰呈黄色。E元素的气态单质、E的最高价氧化物的水化物均能与D的最高价氧化物的水化物反应。
(1)上述4种元素按照原子序数由大到小排列为____、____、____、____;(填元素符号);
(2) B、C形成的化合物(比空气重)的结构式为 ;
(3)C、D的单质在加热条件下生成物质X,其中含有化学键的类型为_____;X的电子式为 ;
(4)Y是C的气态氢化物。常温下,将D的单质投入Y中,发生反应的离子方程式为__________________;该反应__________(填“能”、“不能”)作为设计原电池的反应原理。
试题篮
()