据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是
| A.电池放电时Na+从b极区移向a极区 |
| B.电极b采用MnO2,MnO2既作电极材料又有催化作用 |
| C.每消耗1mol H2O2,转移的电子为1mol |
| D.该电池的正极反应为:BH4-+8OH--8e-=BO2-+6H2O |
下图为某种甲醇燃料电池示意图,工作时电子流方向如图所示。下列判断正确的是
| A.X为氧气 |
| B.电极A反应式:CH3OH-6e-+H2O = CO2+6H+ |
| C.B电极附近溶液pH增大 |
| D.电极材料活泼性:A>B |
某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气。所用燃料为氢气,电解质为熔融的碳酸钾。已知该电池的总反应为2H2+O2==2H2O,正极反应为O2+2CO2+4e-==2CO32—,则下列推断正确的是
| A.负极反应为H2+2OH--2e-==2H2O |
| B.放电时负极有CO2生成 |
| C.该电池供应2 mol水蒸气,同时转移2 mol电子 |
| D.该电池可在常温或高温时进行工作,对环境具有较强的适应性 |
化学家正在研究尿素动力燃料电池,尿液也能发电。用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于描述正确的是
| A.电池工作时H+移向负极 |
| B.该电池用的电解质溶液是KOH溶液 |
| C.甲电极反应式为:CO(NH2)2 + H2O-6e- ═ CO2 + N2 + 6 H+ |
| D.电池工作时,理论每净化1mol CO(NH2)2,消耗33.6 L O2 |
以葡萄糖为燃料的微生物燃料电池示意图如图所示。
关于该电池的叙述正确的是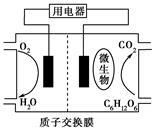
| A.该电池能够在高温下工作 |
| B.电池的负极反应为: C6H12O6+6H2O-24e-=6CO2↑+24H+ |
| C.放电过程中,H+从正极区向负极区迁移 |
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体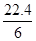 L L |
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl = Na2Mn5O10+2AgCl 下列“水” 电池在海水中放电时的有关说法正确的是( )
| A.正极反应式:Ag+Cl--e-="=" AgCl |
| B.每生成1 mol Na2Mn5O10转移2 mol电子 |
| C.Na+不断向“水”电池的负极移动 |
| D.AgCl是还原产物 |
铅蓄电池是典型的可充电电池,它的正负极隔板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O(如图),则下列说法正确的是
2PbSO4+2H2O(如图),则下列说法正确的是
| A.放电时负极反应是:Pb-2e-=Pb2+,充电是阴极反应是:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
| B.闭合K断开K1,电流的流动方向是从B到A |
| C.放电过程中,溶液的pH不断减小 |
| D.放电时,线路上若有1mole-通过,则消耗硫酸也是1mol |
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
| A.正极反应为Cl2+2e-=2Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.01 mol离子 |
甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成.电池的总反应式为2CH3OH+3O2+4OH-═2CO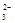 +6H2O.则下列说法正确的是
+6H2O.则下列说法正确的是
| A.电池放电时通入空气的电极为负极 |
| B.电池放电时负极的电极反应式为CH3OH-6e-+H2O═CO2↑+6H+ |
C.由于CO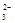 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 |
| D.电池放电时每消耗1molCH3OH转移6mol电子 |
已知某碱性硼化钒(VB3)一空气电池工作时发生反应为:11O2+4VB2=2V2O5+4B2O3。以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
| A.VB2电极发生的电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ |
| B.若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L |
| C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D.外电路中电子由a电极流向b电极 |
锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时的电极反应式为
负极反应:C6Li-xe-=C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成的复合材料)
正极反应:Li1-xMO2+xLi++x e-=LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是( )
| A.锂离子电池放电时电池反应为LiMO2+C6Li1-x=C6Li+Li1-xMO2 |
| B.锂离子电池充电时电池内部Li+向负极所连的电极移动 |
| C.锂离子电池放电时电池内部电流从负极流向正极 |
| D.锂离子电池充电时阳极反应为C6Li1-x+xLi++xe-=C6Li |
已知电池的比能量是参与电极反应的单位质量的电极材料放出电能的大小。有关下述两种电池说法正确的是( )

锂离子电池的总反应为:LixC+Li1-xCoO2 C+LiCoO2
C+LiCoO2
锂硫电池的总反应为:2Li+S Li2S
Li2S
| A.锂离子电池放电时,Li+向负极迁移 |
| B.锂硫电池充电时,锂电极发生还原反应 |
| C.理论上两种电池的比能量相同 |
| D.右图表示用锂离子电池给锂硫电池充电 |
NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
| A.O2在石墨Ⅱ附近发生氧化反应 |
| B.该电池放电时NO3-向石墨Ⅱ电极迁移 |
C.石墨Ⅰ附近发生的反应:3NO2 +2e- NO+ 2NO3- NO+ 2NO3- |
| D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1 |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料的说法正确的是 ( )
| A.在熔融电解质中,OH-由正极移向负极 |
| B.电池的总反应是:2C4H10+13O2→8CO2+10H2O |
| C.通入空气的一极是正极,电极反应为:O2+2H2O +4e-=4OH- |
| D.通入丁烷的一极是正极,电极反应为:C4H10+26 e-+13O2-=4 CO2↑+5 H2O |
试题篮
()