右图是一种正在投入生产的大型蓄电系统的原理图。电池的中间为只允许钠离子通过的离子选择性膜。电池充、放电的总反应方程式为:2Na2S2+NaBr3 Na2S4+3NaBr
Na2S4+3NaBr
下述关于此电池说法正确的是
| A.充电的过程中当O.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子 |
| B.电池放电时,负极反应为:3NaBr一2e-=NaBr3+2Na |
| C.充电过程中,电极a与电源的正极相连 |
| D.放电过程中钠离子从右到左通过离子交换膜 |
在固态金属氧化物电解池中,高温电解H2O﹣CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
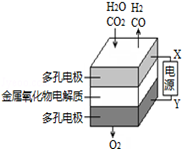
| A.X是电源的负极 |
| B.阴极的反应式是:H2O+2e﹣═H2+O2﹣,CO2+2e﹣═CO+O2﹣ |
C.总反应可表示为:H2O+CO2 H2+CO+O2 H2+CO+O2 |
| D.阴、阳两极生成的气体的物质的量之比是1:1 |
一种使用阴离子交换膜(只也许阴离子通过)的铜锌电池结构如下图:
以下选项两栏内容正确且相关联的是
| 选项 |
操作与现象 |
解释与推论 |
| A |
电池放电时化学能转化为电能 |
Zn(s) + Cu2+(aq) = Zn2+ + Cu(s) △H>0 |
| B |
该电池充电时铜棒变细 |
两电极区溶液颜色都变深 |
| C |
该电池放电时铜棒是电池正极 |
Cl-通过交换膜从左(铜棒区)向右(锌棒区)移动 |
| D |
该电池充电时a接电源正极 |
电极反应Cu2++2e- = Cu |
已知:锂离子电池的总反应为: C+LiCoO2;锂硫电池的总反应为:2Li+S
C+LiCoO2;锂硫电池的总反应为:2Li+S Li2S有关上述两种电池说法正确的是( )
Li2S有关上述两种电池说法正确的是( )

| A.锂离子电池放电时,Li+向负极迁移 |
| B.锂硫电池充电时,锂电极发生还原反应 |
| C.理论上两种电池的比能量相同 |
| D.右图中表示用锂离子电池给锂硫电池充电 |
一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:
CH3CH2OH+O2=CH3COOH+H2O。下列有关说法不正确的是
| A.检测时,电解质溶液中的H+向正极移动 |
| B.若有0.4mol电子转移,则消耗2.24L氧气 |
| C.正极上发生还原反应,负极上发生氧化反应 |
| D.负极上的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
微生物燃料电池(Microbial Fuel Cell,MFC)是一种利用微生物将有机物中的化学能直接转化成电能的装置。最早用于有机废水处理,下图是利用微生物燃料电池处理含甲醛废水的装置,其中3是质子交换膜,下列有关说法不正确的是
A.负极发生的反应为:HCHO-4e-+H2O=CO2+4H+
B.负极所在的左室中需保持厌氧环境
C.O2参与正极反应,发生还原反应
D.NH4+通过循环操作最终被转化成N2
微型纽扣电池在现代生活中是广泛应用的一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应式分别为:Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-,电池总反应式为Ag2O+Zn===2Ag+ZnO。根据上述反应式,判断下列叙述中正确的是
| A.在使用过程中,电池负极区溶液pH增大 |
| B.在使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 |
| D.外电路中每通过0.2 mol电子,正极的质量理论上减小1.6 g |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是( )

A.当有0.1 mol电子转移时,a极产生1.12 L O2(标况)
B.b极上发生的电极反应是:2H + 2e- = H2↑
+ 2e- = H2↑
C.d极上发生的电极反应是:O2 + 4H+ + 4e- = 2H2O
D.c极上进行还原反应,B中的H+可以通过隔膜进入A
甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成.电池的总反应式为2CH3OH+3O2+4OH-═2CO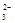 +6H2O.则下列说法正确的是
+6H2O.则下列说法正确的是
| A.电池放电时通入空气的电极为负极 |
| B.电池放电时负极的电极反应式为CH3OH-6e-+H2O═CO2↑+6H+ |
C.由于CO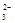 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 水解显碱性,电池放电时,电解质溶液的pH逐渐增大 |
| D.电池放电时每消耗1molCH3OH转移6mol电子 |
已知某碱性硼化钒(VB3)一空气电池工作时发生反应为:11O2+4VB2=2V2O5+4B2O3。以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
| A.VB2电极发生的电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ |
| B.若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L |
| C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D.外电路中电子由a电极流向b电极 |
锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时的电极反应式为
负极反应:C6Li-xe-=C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成的复合材料)
正极反应:Li1-xMO2+xLi++x e-=LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是( )
| A.锂离子电池放电时电池反应为LiMO2+C6Li1-x=C6Li+Li1-xMO2 |
| B.锂离子电池充电时电池内部Li+向负极所连的电极移动 |
| C.锂离子电池放电时电池内部电流从负极流向正极 |
| D.锂离子电池充电时阳极反应为C6Li1-x+xLi++xe-=C6Li |
已知电池的比能量是参与电极反应的单位质量的电极材料放出电能的大小。有关下述两种电池说法正确的是( )

锂离子电池的总反应为:LixC+Li1-xCoO2 C+LiCoO2
C+LiCoO2
锂硫电池的总反应为:2Li+S Li2S
Li2S
| A.锂离子电池放电时,Li+向负极迁移 |
| B.锂硫电池充电时,锂电极发生还原反应 |
| C.理论上两种电池的比能量相同 |
| D.右图表示用锂离子电池给锂硫电池充电 |
NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
| A.O2在石墨Ⅱ附近发生氧化反应 |
| B.该电池放电时NO3-向石墨Ⅱ电极迁移 |
C.石墨Ⅰ附近发生的反应:3NO2 +2e- NO+ 2NO3- NO+ 2NO3- |
| D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1 |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料的说法正确的是 ( )
| A.在熔融电解质中,OH-由正极移向负极 |
| B.电池的总反应是:2C4H10+13O2→8CO2+10H2O |
| C.通入空气的一极是正极,电极反应为:O2+2H2O +4e-=4OH- |
| D.通入丁烷的一极是正极,电极反应为:C4H10+26 e-+13O2-=4 CO2↑+5 H2O |
试题篮
()