下图为铅蓄电池的示意图。下列说法正确的是
| A.放电时,N为负极,其电极反应式为:PbO2+SO42-+4H++2e-=PbSO4+2H2O |
| B.放电时,c(H2SO4)不变,两极的质量增加 |
| C.充电时,阳极反应式为:PbSO4+2e-= Pb+SO42- |
| D.充电时,若N连电源正极,则该极生成PbO2 |
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:xMg+Mo3S4 MgxMo3S4,下列说法正确的是
MgxMo3S4,下列说法正确的是
| A.电池放电时,Mg2+向负极迁移 |
| B.电池放电时,正极反应为Mo3S4+2xe﹣+xMg2+=MgxMo3S4 |
| C.电池充电时,阴极发生还原反应生成Mo3S4 |
| D.电池充电时,阳极反应为xMg﹣2xe﹣=xMg2+ |
(14分)工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键的步骤。
(1)一定条件下,SO2可发生反应:SO2(g)+ O2(g)
O2(g) SO3(g) △H=﹣98kJ·mol﹣1。
SO3(g) △H=﹣98kJ·mol﹣1。
①某温度下,在100 L的恒容密闭容器中开始加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出热量196 kJ,该温度下平衡常数K=_______(用分数表示)。
②上述反应按照相同的物质的量投料,测得SO2在不同温度下的平衡转化率a%与压强的关系如下图所示。下列说法正确的是_______(填序号)。
| A.温度:T3>T2>T1 |
| B.正反应速率:v(c)>v(a),v(b)>v(d) |
| C.平衡常数:K(a)>k(c),K(b)=K(d) |
| D.平均摩尔质量:M(a)>M(c),M(b)>M(d) |
③上述反应达平衡后,保持温度和容器的压强不变,若再通入一定量SO3(g),则SO2的体积分数_______(填“增大”、“减小”、“不变”)。
(2)某人设想以下图所示装置用电化学原理模拟生产硫酸: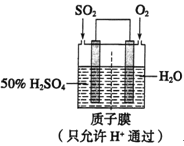
①通入O2的电极是________极。
②写出通入SO2的电极的电极反应式:_______________
③若此过程中转移了0.2mol电子,则质子膜两侧电解液的质量变化差(△m左﹣△m右)为________g(忽略气体的溶解)。
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2 +O2→2CH3CHO。
下列有关说法正确的是
| A.电子移动方向:电极a→磷酸溶液→电极b |
| B.正极反应式为:CH2=CH2-2e- + 2OH- = CH3CHO + H2O |
| C.每有0.1mol O2反应,则迁移H+ 0.4mol |
| D.该电池为可充电电池 |
A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B的最高价含氧酸可与其气态氢化物反应生成盐,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。用元素符号或化学式回答下列问题。
(1)X在周期表中的位置是 ;五种元素的原子半径从大到小的顺序是 ;化合物Y2X2的电子式为 。
(2)X、Z的简单氢化物中沸点较高的是 ;原因是 。
(3)A与X和A与Z均能形成18个电子的化合物,这两种化合物发生反应可生成Z,其反应的化学方程式为:_________________________;
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为:_____________。
(5)写出化合物Y2X2与水反应的离子方程式:_________________________。
烃A在一定条件下可以按下图进行转化: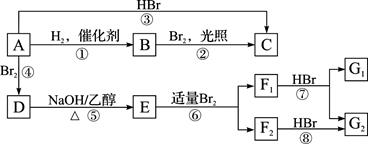
已知D为 ,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体。据此作答:
,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体。据此作答:
(1)框图中属于取代反应的是_______(填序号);B完全燃烧后生成的CO2和水的质量比为_________。
(2)A的结构简式是_________________;G1的结构简式是____________________。
(3)写出E在一定条件下生成高聚物的化学方程式:____________________
(4)已知B可在碱性条件下和O2构建成燃料电池,写出负极的电极反应式:___________________
汽车的启动电源常用铅蓄电池,该电池在放电时的反应如下:Pb (s)+ PbO2(s) +2H2SO4(aq) 2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是
2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb(s)+SO42-(aq)–2e – = PbSO4(s) |
| C.铅蓄电池属于一次电池 |
| D.电池放电时,溶液酸性增强 |
一种氢氧燃料电池用30%KOH溶液为电解质溶液,有关这种电池的说法中错误的是
| A.H2在负极发生氧化反应 | B.供电时的总反应为:2H2 + O2 = 2H2O |
| C.产物为无污染的水,属于环境友好电池 | D.负极反应为:H2 - 2e- = 2H+ |
可以将氧化还原反应2H2+O2=2H2O设计成原电池。(每空2分)
(1)利用H2、O2、HCl溶液构成燃料电池,则正极的电极反应式为_______________;负极的电极反 应式为________________。
(2)把H2改成CH4,KOH溶液作电解质,则负极的电极反应式为_______________,当导线中通过4 mol电子时,需消耗______mol的KOH;将4 mol CH4完全与Cl2发生取代反应,并生成等物质的量的四种氯代物,则理论上需要消耗Cl2的物质的量为_______mol。
某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气。所用燃料为氢气,电解质为熔融的碳酸钾。已知该电池的总反应为2H2+O2==2H2O,正极反应为O2+2CO2+4e-==2CO32—,则下列推断正确的是
| A.负极反应为H2+2OH--2e-==2H2O |
| B.放电时负极有CO2生成 |
| C.该电池供应2 mol水蒸气,同时转移2 mol电子 |
| D.该电池可在常温或高温时进行工作,对环境具有较强的适应性 |
硫化氢(H2S)是一种有毒的可燃性气体,用H2S、空气和KOH溶液可以组成燃料电池,其总反应式为2H2S+3O2+4KOH==2K2SO3+4H2O。
(1)该电池工作时正极应通入 。
(2)该电池的负极电极反应式为: 。
(3)该电池工作时负极区溶液的pH (填“升高”“不变”“降低”)
(4)有人提出K2SO3可被氧化为K2SO4,因此上述电极反应式中的K2SO3应为K2SO4,某学习小组欲将电池工作一段时间后的电解质溶液取出检验,以确定电池工作时反应的产物。实验室有下列试剂供选用,请帮助该小组完成实验方案设计。
0.01mol·L-1KMnO4酸性溶液,1mol·L-1HNO3,1mol·L-1H2SO4,1mol·L-1HCl,0.1mol·L-1Ba(OH)2,0.1 mol·L-1 BaCl2。
| 实验步骤 |
实验现象及相关结论 |
| ①取少量电解质溶液于试管中,用pH试纸测其pH。 |
试纸呈深蓝色,经比对溶液的pH约为14,说明溶液中有残余的KOH。 |
| ②继续加入( )溶液,再加入( )溶液,振荡。 |
若有白色沉淀产生,则溶液中含有K2SO4。 若无白色沉淀产生,则溶液中没有K2SO4 |
| ③另取少量电解质溶液于试管中,先加1 mol·L-1的H2SO4酸化,再滴入2~3滴0.01 mol·L-1KMnO4酸性溶液,振荡 |
( ) |
(5)若电池开始工作时每100mL电解质溶液含KOH 56g,取电池工作一段时间后的电解质溶液20.00mL,加入BaCl2溶液至沉淀完全,过滤洗涤沉淀,将沉沉在空气中充分加热至恒重,测得固体质量为11.65g,计算电池工作一段时间后溶液中KOH的物质的量浓度( )。
(结果保留四位有效数字,假设溶液体积保持不变,已知:M(KOH)=56,M(BaSO4)=233,M(BaSO3)=217)
近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法正确的是
| A.碳极发生的反应是:2H2O+O2+4e-=4OH- |
| B.有机电解质通过固体电解质可进入水溶液中 |
| C.理论上外电路中每转移1mol电子,负极消耗的质量为7g |
| D.该电池如可以充电,充电时碳极接外加电源的负极,锂极接外加电池的正极 |
铅蓄电池是典型的可充电电池,它的正负极隔板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O(如图),则下列说法正确的是
2PbSO4+2H2O(如图),则下列说法正确的是
| A.放电时负极反应是:Pb-2e-=Pb2+,充电是阴极反应是:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
| B.闭合K断开K1,电流的流动方向是从B到A |
| C.放电过程中,溶液的pH不断减小 |
| D.放电时,线路上若有1mole-通过,则消耗硫酸也是1mol |
如图所示是一个燃料电池的示意图,当此燃料电池工作时,下列分析中正确的是
| A.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+ |
| B.如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通 O2的电极上发生的反应为:O2+4e-+2H2O=4OH- |
| C.如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的 反应为:CH4-8e-+10OH-=CO32-+7H2O |
| D.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动 |
一种新型燃料电池,一极通入空气,另一极通入丁烷;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是
| A.在熔融电解质中,O2-由负极移向正极 |
| B.通入丁烷的一极是正极,电极反应为:C4H10+26e-+13O2-=4CO2+5H2O |
| C.通入空气的一极是负极,电极反应为:O2+4e-=2O2- |
| D.电池的总反应是:2C4H10+13O2=8CO2+10H2O |
试题篮
()