向20mL 0.1mol/L NH4HSO4溶液中滴入0.1mol/L NaOH溶液,下列说法正确的是
| A.整个反应过程中:c(H+) + c(Na+) + c(NH4+)=c(OH-) + c(SO42-) |
| B.当滴入30mL NaOH溶液时(pH>7):c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+) |
| C.当滴入20mL NaOH溶液时:2c(SO42-)=c(NH3·H2O)+ c(NH4+) |
| D.当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)= c(OH-) |
常温下,用NaOH溶液滴定20.00mL0.1 mol•L-1CH3COOH溶液所得滴定曲线如图,下列说法正确的是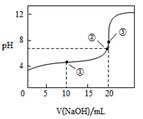
| A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
| B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
| C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
常温下,下列溶液中的离子浓度关系正确的是
| A.pH=3的醋酸溶液中:c(H+)=c(CH3COO-)="3.0" mol•L-1 |
| B.Na2S溶液中:c(Na+)>c(HS-)>c(OH-)>c(H2S) |
| C.pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
下列叙述不正确的是
A.0.1 mol•L-1氨水中,c(OH-)>c(NH4+)
B.等体积等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
C.在0.1 mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.0.1 mol•L-1某二元弱酸强碱盐Na2A溶液中,c(Na+)=2c(A2-)+2c(HA-)+2c(H2A)
已知0.1 mol•L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.物质的量浓度相等的Na2A、NaHA两溶液的pH相大小为前者小于后者
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
下列有关说法正确的是( )
| A.常温下,0.1 mol/L Na2S溶液中存在:c(OH-) = c(H+) + c(HS-) + c(H2S) |
| B.常温下,pH为1的0.1 mol/L HA溶液与0.1 mol/L NaOH溶液恰好完全反应时,溶液中一定存在: c (Na+) = c(A-) > c(OH-) = c(H+) |
| C.常温下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)="0.1" mol/L: c(Na+) = c(CH3COOH) > c(CH3COO-) > c(H+) = c(OH-) |
D.常温下,将0.1 mol/L CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中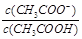 的值减小到原来的 的值减小到原来的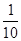 |
一定温度下,下列溶液的离子浓度关系式正确的是( )
| A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1 |
| B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合: c(Na+)+c(H+)=c(OH-)+c(HC2O4-) |
| D.pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③ |
室温下,在0.2 mol·L-1 Al2(SO4)3溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )

A.a点时溶液呈酸性的原因是Al3+水解,离子方程式为Al3++3OH- Al(OH)3 Al(OH)3 |
| B.a~b段,溶液pH增大,Al3+浓度不变 |
| C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| D.d点时,Al(OH)3沉淀开始溶解 |
现有物质的量浓度均为 0.1 mol·L - 1 的四种溶液各25mL:①氨水 ②NH4Cl 溶液
③Na2CO3溶液 ④NaHCO3溶液,下列说法正确的是:
| A.4种溶液pH的大小顺序:①>④>③>② |
| B.①、②混合后pH>7,则混合溶液中c(NH4+)<c(NH3·H2O) |
| C.①、②中分别加入25mL 0.1 mol·L – 1盐酸后,溶液中c(NH4+):①>② |
| D.③、④中分别加入12.5mL 0.1 mol·L – 1NaOH溶液后,两溶液中离子种类相同 |
下列溶液中粒子的物质的量浓度关系正确的是:
| A.0.1 mol·L - 1 NaHC2O4溶液与0.1 mol·L – 1KOH溶液等体积混合,所得溶液中: c(Na+)>c(K+) >c(C2O42-) >c(OH-) >c(HC2O4-) |
| B.20mL 0.1 mol·L - 1NH4Cl溶液与10mL 0.1 mol·L - 1NaOH溶液混合后溶液呈碱性,所得溶液中:c(Cl-)>c(NH4+) >c(Na+)>c(OH-)>c(H+) |
| C.常温下,pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中: c(Na+)+ c(OH-) >c(H+)+ c(F-) |
| D.0.1 mol·L – 1 NH3·H2O溶液与0.1 mol·L – 1 HNO3溶液等体积混合,所得溶液中: |
c(H+) >c(OH-) + c(NH3·H2O)
下列有关电解质溶液中粒子浓度关系正确的是
| A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) |
| B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C.CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-) |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
HA为酸性略强于醋酸的一元弱酸,在0.1 mol·L-1 NaA溶液中,离子浓度关系正确的是
| A.c(Na+)>c(A-)>c(H+)>c(OH-) |
| B.c(Na+)>c(OH-)>c(A-)>c(H+) |
| C.c(Na+)+c(H+)=c(A-)+c(OH-) |
| D.c(Na+)+c(OH-)=c(A-)+c(H+) |
为了使Na2S溶液中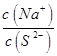 的比值变小,可采取的措施是
的比值变小,可采取的措施是
①适量盐酸 ②适量NaOH(s) ③适量KOH(s) ④适量KHS(s)
⑤加水 ⑥通H2S(g) ⑦加热
| A.③④ | B.①②⑤⑥⑦ | C.②③ | D.②③④ |
物质的量浓度相同时,下列既能跟NaOH溶液反应,又能跟盐酸反应的溶液中,pH最大的是
| A.Na2CO3溶液 | B.NH4HCO3溶液 | C.NaHSO4溶液 | D.NaHSO3溶液 |
试题篮
()