下列有关硫酸和硝酸的叙述正确的是( )
| A.将浓硫酸和浓硝酸分别长期露置在空气中,浓度均会降低 |
| B.在常温下,浓硫酸和浓硝酸均能与铜剧烈反应 |
| C.稀硫酸和稀硝酸分别与金属反应时,S和N的化合物都会发生变化 |
| D.因为浓硫酸和浓硝酸都能与铁反应,所以常温下二者都不能用铁剂容器盛装 |
以下物质间的每步转化都是通过一步反应能实现的是
| A.Al→Al2O3→Al(OH)3→NaAlO2 | B.Fe→FeO→Fe(OH)2→Fe(OH)3 |
| C.S→SO3→H2SO4→MgSO4 | D.N2→NO→NO2→HNO3 |
除去下表内各物质中含有的少量杂质,写出除杂试剂,并填写分离方法。
| 序号 |
物质 |
杂质 |
所加试剂 |
分离方法 |
| (1) |
NO |
NO2 |
|
|
| (2) |
Fe粉 |
Al粉 |
|
|
| (3) |
氯化钠固体 |
氯化铵固体 |
|
|
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
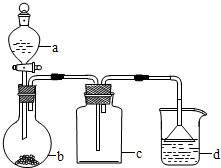
| 选项 |
a中的物质 |
b中的物质 |
c中收集的气体 |
d中的物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓硫酸 |
Na2SO3 |
SO2 |
NaOH溶液 |
| C |
稀硝酸 |
Cu |
NO2 |
H2O |
| D |
饱和食盐水 |
MnO2 |
Cl2 |
NaOH溶液 |
下列说法正确的是( )
| A.浓硫酸用铜制容器密封保存 | B.SO2能使溴水褪色,体现其漂白性 |
| C.氨气是电解质,因为氨气的水溶液能导电 | D.光导纤维的主要成分是二氧化硅 |
NO、NO2、NH3、SO2、CO等都是空气污染物。
(1)酸雨的形成主要是大气中的_________溶于水后形成了酸性溶液。
(2)在汽车的排气管上装一个催化转化装置,可使汽车尾气中的NO与CO反应,生成氮气和碳的另一种无污染的气体,请完成该转化的化学方程式: NO + CO—N2+ 。
制取氨气并完成喷泉实验
(1)写出实验室制取氨气的化学方程式: 。
(2)收集氨气应使用 法,要制取干燥的氨气可选用 做干燥剂。
(3)如图进行喷泉实验,上部烧瓶已装满干燥的氨气,引发水上喷的操作是 ,该实验的原理是
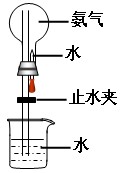
(4)反应后,烧瓶内的溶液中含有的微粒为 。
将含有少量杂质的硝酸铜固体用酒精灯加热至恒重,收集到20.20 mL气体,再将该气体用足量水吸收,剩余2.10 mL气体(气体体积在同温同压下测定),则关于杂质成分的推测不合理的是
| A.NaNO3 | B.Mg(NO3)2 |
| C.AgNO3 | D.NaNO3和AgNO3的混合物 |
下列事实,可以证明氨水是弱碱的是
| A.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁 |
| B.铵盐受热易分解 |
| C.0.1mol/L的氨水可以使酚酞试液变红 |
| D.0.1mol/L的NH4Cl溶液的pH约为5 |
下列说法正确的是
| A.铵盐不稳定,受热分解都产生氨气 |
| B.N2是空气中的主要成分之一,雷雨时可直接转化为NO2 |
| C.由于浓硫酸有强氧化性,因此不能用铁罐贮存浓硫酸 |
| D.Cl2与石灰乳反应可以制得含氯漂白剂 |
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体,现将此无色混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色,对于原混合气体成分的判断中正确的是
| A.肯定有NO和NO2 | B.肯定有SO2和NO |
| C.可能有Cl2和O2 | D.肯定没有Cl2、NO2,可能有O2 |
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| |
X. |
Y |
Z |
| ① |
NaOH溶液 |
Al(OH)3 |
稀硫酸 |
| ② |
KOH溶液 |
SiO2 |
浓盐酸 |
| ③ |
O2 |
N2 |
H2 |
| ④ |
FeCl3溶液 |
Cu |
浓硝酸 |
A.①③ B.①④ C.②④ D.②③
试题篮
()