化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是( )
| A.大量排放NO和NO2等氮氧化物是形成光化学烟雾和酸雨的一个重要原因 |
| B.采用纳米二氧化钛光触媒技术,将汽车尾气中的NO和CO转化为无害气体 |
| C.高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遭遇强碱会“断路” |
| D.大量燃烧化石燃料排放的废气中含大量SO2 ,从而使雨水的PH=5.6,形成酸雨 |
氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是( )
| A.氮氧化铝中氮的化合价是-3 |
| B.反应中氮气作氧化剂 |
| C.反应中每生成5.7g AlON 同时生成1.12 L CO |
| D.反应中氧化产物和还原产物的物质的量之比是2:1 |
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
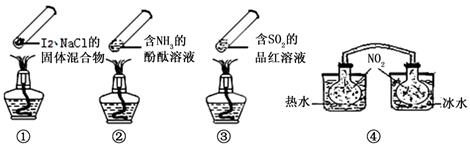
| A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差 |
| B.加热时,②、③中的溶液均变红,冷却后又都变为无色 |
| C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
| D.四个“封管实验”中都有可逆反应发生 |
右图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )
| 选项 |
X |
收集气体 |
 Y Y |
| A |
碱石灰 |
氯化氢 |
水 |
| B |
碱石灰 |
氨气 |
水 |
| C |
氯化钙 |
二氧化硫 |
氢氧化钠 |
| D |
氯化钙 |
一氧化氮 |
氢氧化钠 |
现将1mo1Cu2S与144g FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2、CuSO4的混合溶液,并产生NO气体。则最终反应所得NO物质的量为
| A.4 mo1 | B.5 mo1 | C.6 mo1 | D.7 mo1 |
a mol Cu与含b mol HNO3的溶液恰好完全反应,则被还原的HNO3的物质的量一定是
| A.(b-2a) mol | B. mol mol |
C. mol mol |
D.2a mol |
下列反应中,硝酸既表现酸性,又表现氧化性的是
| A.Fe(OH)2跟稀硝酸反应 |
| B.Fe2O3跟稀硝酸反应 |
| C.CuO跟稀硝酸反应 |
| D.Al(OH)3跟稀硝酸反应 |
无色的混合气体甲,可能含有NO、CO2、NO2、NH3、N2中的某几种。将100mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余。则甲气体的组成为
| A.NH3、NO、CO2 | B.NH3、NO2、N2 |
| C.NH3、NO2、CO2 | D.NO、CO2、N2 |
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想,其中不成立的是
| A.Mg(NO3)2、NO2、O2 | B.MgO、NO2、O2 | C.Mg3N2、O2 | D.MgO、NO2、N2 |
将NO2、NH3、O2混合气22.4L通过稀硫酸后,溶液质量增加了26.7g,气体体积缩小为4.48L。(气体体积均在标况下测定)剩余气体能使带火星的木条着火,则混合气体的平均相对分子质量为(4NO2+O2+2H2O=4HNO3)( )
| A.28.1 | B.30.2 | C.33.1 | D.34.0 |
在某稀溶液中含有0.1mol HNO3和x mol H2SO4,向其中加入9.6 g铜粉,充分反应后产生的气体在标准状况下的体积为2.24L,则x值至少为 ( )
| A.0.1 | B.0.12 | C.0.15 | D.0.2 |
同温同压下,在3支体积不同的试管中分别充满等体积混合的2种气体,它们是:①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中溶质的物质的量浓度分别为c1、c2、c3(假设溶质全在试管中),则下列关系正确的是
| A.c1>c2>c3 | B.c1>c3>c2 | C.c1=c3>c2 | D.c1=c2>c3 |
下列有关硝酸化学性质的叙述中,正确的是 ( )
| A.敞口放置的浓硝酸浓度变小是因为浓硝酸的吸水性 |
| B.硝酸可与Na2SO3反应制得SO2气体 |
| C.浓硝酸因分解放出的NO2又溶解于硝酸而呈黄色 |
| D.硝酸能与Fe2O3反应,表现氧化性 |
试题篮
()