A、B、C、D、E、F、G、H八种物质间存在着如下图所示的变化关系,其中A、B为单质,相对分子质量A大于B;E在通常状况下为有颜色,有刺激性气味的气体;H为一种氯化物,与碱石灰共热可制取C;G中含A元素35%。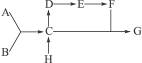
完成下列问题:
(1)用化学式表示各物质。
(2)写出C D的化学方程式,并标出电子转移方向和数目。
D的化学方程式,并标出电子转移方向和数目。
常温下,有一无色混合气体,可能由Cl2、HCl、NO、O2、CO2、N2、H2、NH3中的两种或多种组成,取此混合气体200 mL进行实验如下:
(1)将此气体通过浓硫酸,体积减少40 mL;
(2)剩余气体通过足量过氧化钠固体,体积又减少40 mL;
(3)剩余气体仍为无色,引燃后冷却至常温,体积又减少105 mL;
(4)最后剩余气体为15 mL,经分析知道其中氧气占1/3。则原混合气体中一定不含________;一定含________,其体积分别是_________。
各取一定量的NaHCO3和NH4HCO3分别加热到300 ℃使之完全分解,在该温度和压强下收集到的气体体积之比是1∶6,则原来NaHCO3和NH4HCO3的物质的量之比是________________。
在标准状况下,把一个装有氨气的集气瓶通过带活塞的玻璃管,倒立于有足量水的水槽中作喷泉实验。水喷入烧瓶,形成了氨水溶液,因此烧瓶中氨水的物质的量浓度为___________,溶质的质量分数为_______________。
要制取H2、O2、Cl2、HCl、NH3、H2S,从下列各物质中,分别选出必要的物质,将序号填在括号内。
a.硫化亚铁 b.浓硫酸 c.浓盐酸 d.二氧化锰
e.硝酸钠 f.铜片 g.氯化铵 h.锌 i.浓硝酸
j.氢氧化钙 k.稀硫酸 l.食盐晶体 m.氯酸钾
n.稀硝酸 o.高锰酸钾
制H2______________,制O2______________,制Cl2______________,制HCl______________,
制NH3_____________,制H2S______________。
上述气体中最不适于用排水法收集的是______________;最不适于用浓硫酸干燥的是______________;最适于用向上排气取气法收集的是______________。
在铂催化剂和加热的条件下,氨气与氧气反应的化学方程式为_______________________,氧化剂是__________,还原剂是__________,若参加反应的NH3为6 mol,则反应中转移了__________mol电子。
有一瓶无色干燥的混合气体,可能由HCl、NO、NO2、CO2、NH3、N2和O2中的几种混合而成。
(1)将混合气体通过浓H2SO4时,气体体积明显减少。
(2)再通过碱石灰时,体积又明显减少。
(3)剩余气体接触空气后,很快变成红棕色。
试推断此混合气体中,一定有_________,一定没有__________,可能含有__________。
已知A、B、C、D均为短周期元素,它们的原子序数依次递增。A是最外层为一个电子的非金属元素,C原子的最外层电子数是次外层的3倍;C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物。由A、B、C三种元素可形成离子晶体,该晶体中各元素原子的物质的量之比为A∶B∶C=4∶2∶3。请完成下列问题:
(1)画出B的原子结构示意图______________;写出C和D形成的淡黄色固体化合物的电子式______________。
(2)元素原子的物质的量之比为A∶B∶C=4∶2∶3的晶体名称为______________,其水溶液显______________性,其反应的离子方程式为_______________________________。
(3)请写出与A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两元素组成的粒子符号(举两例)______________。
(4)写出由B、C元素组成且元素原子质量比为B∶C=7∶12的化合物的化学式_______。
NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。请完成下列问题:
(1)NO对环境的危害在于_______(填以下项的编号)。( )
| A.破坏臭氧层 |
| B.高温下能使一些金属被氧化 |
| C.造成酸雨 |
| D.与人体血红蛋白结合 |
(2)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式_____________________。
(3)在常温下,把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50 ℃,发现气体的压力迅速下降,压力降至略小于原压力 就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式______________________。
就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式______________________。
(4)解释变化(3)中为什么最后的气体总压力小于原压力的 。
。
80℃,101.3 kPa下,用图86装置进行如下实验。A、C两筒内分别装有无色气体,它们可能是NH3、O2、N2、H2S、NO、CO2等气体,B筒内装有Na2O2固体,推动A的活塞使A筒内气体缓缓地全部通过B后进入C筒,C筒内气体由无色变为红棕色,但其体积换算成同温同压下却并未变化(不考虑2NO2 N2O4)。
N2O4)。
图8-6
(1)C中发生的反应,其化学方程式是 。已知原C中的气体是单一气体,它是 ,理由是 。
(2)将反应后C筒内气体用水充分吸收,在同温同压下,气体体积减少一半,则与水反应前 C中的气体是 。
(3)若实验开始前A、C中气体体积(换算成标准状况)分别为1.40 L和2.24 L,且A中的气体经过B管后,B管增重了1.40 g。经计算和推理可判定A中的气体是 ,其质量为 g(不必写出计算和推理过程)。
在春夏之交的夜晚,墓地周围常出现“鬼火”,即磷火,这是尸骨中的Ca3P2与水反应生成PH3,PH3自燃的结果,写出Ca3P2与水反应的化学方程式:__________,再写出PH3发生自燃的化学方程式:_______________。
(1)舞台上的幕布与布景多是用浓NH4Cl溶液浸过制成的,可以防火,其原因是_____________________________。
(2)已知NH3结合H+的能力比结合Ag+的能力强。要使[Ag(NH3)2]+转化为自由的Ag+,应加入的试剂是_______,实现转化的离子方程式为______________________________________。
(3)氮的氧化物NOx与NH3反应生成N2和H2O,若在标准状况下1.5 L NOx和2 L NH3恰好完全作用,写出反应的化学方程式:____________________________,NOx中x值为___________。
根据下列变化进行推断:
已知强热A产生的气态物质的平均相对分子质量为26.3。
(1)推断A、B、C、D的化学式:A____________、B____________、C____________、D____________。
(2)写出①②变化的离子方程式。
一种无色澄清溶液可能含有K+、SO 、NH
、NH 、Ba2+、H2PO
、Ba2+、H2PO 、NO
、NO 中的一种或几种,分别取少量溶液进行下列实验:①此溶液加入NaOH溶液有沉淀产生,加热产生一种使湿润红色石蕊试纸变蓝的气体。②另取原溶液浓缩后加入浓硫酸、铜片并加热,产生红棕色气体。由此可知此溶液中一定含有_______离子,一定不含有_______离子。
中的一种或几种,分别取少量溶液进行下列实验:①此溶液加入NaOH溶液有沉淀产生,加热产生一种使湿润红色石蕊试纸变蓝的气体。②另取原溶液浓缩后加入浓硫酸、铜片并加热,产生红棕色气体。由此可知此溶液中一定含有_______离子,一定不含有_______离子。
试题篮
()