(1)实验室制NH3的反应方程式为_____________________________________
(2)氨的催化氧化是工业制取硝酸的基础,写出化学反应方程式。
(3)硝酸具有强氧化性,它能和许多物质发生反应。写出浓硝酸与非金属单质碳的反应方程式。
(4)写出稀硝酸与金属银在加热条件下的反应方程式 _______________________________________________________
某同学用12.5 mol/L浓硝酸来配制500 mL1 mol/L的稀硝酸,并进行有关实验。请回答有关问题:
(1)需要量取12.5 mol/L的浓HNO3________mL,配制该稀硝酸时使用的仪器除量筒、玻璃棒、烧杯外,还必须用到的仪器有______、___________等。
(2)取所配制的稀HNO3200 mL,与一定质量的铜粉充分反应,铜粉全部溶解后,生成的唯一还原产物NO气体在标况下的体积为0.56L。则:写出Cu与稀HNO3反应的化学方程式 ,参加反应的铜粉的质量为_________g。
(3)若要将溶液中Cu2+全部转化为Cu(OH)2沉淀,至少需加入0.2mol/L的NaOH溶液的体积为 ml.
(注:要求在答题卡最下面方框内仅列出计算比例式)
资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是______;碱石灰的作用是______。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:氨催化氧化的化学方程式是____________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是___________;其理由是___________________。
②氨气燃烧的化学方程式是________________________。
已知: NO3-+4H++3e-→NO+2H2O 。现有四种物质:KMnO4、Na2CO3、Cu2O、Fe2(SO4)3,其中能使上述还原过程发生的是 (填化学式),写出该反应化学方程式中氧化产物的化学计量数(写方框内)及其化学式□ 。1mol该物质与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: 。
实验室常用硫酸铝溶液和氨水反应制取氢氧化铝,其离子方程式为 ;
溶液中得到的氢氧化铝是______色______状物质。它是______溶于水的______性化合物,既能与______反应,又能与______反应,其离子方程式分别是 、 。
如图所示为A、B、C、D、E五种含氮物质相互转化的关系图,其中A、B、C、D常温下都是气体,B为红棕色,写出各步反应的化学方程式。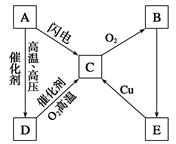
A→C:______________________________________,
D→C:_______________________________________,
B→E:_______________________________________,
E→C:_______________________________________。
将1.92 g铜置入一定量的浓硝酸中,并微热,随着铜的不断减少,反应生成的气体颜色逐渐变浅,当铜反应完毕时(铜片完全消失),共收集到标况下气体1.12 L(设不含N2O4),求:
(1)收集到的气体中主要有含有 ;
(2)上述过程中,有关反应的化学方程式为 ; ;
(3)反应中被还原的HNO3的物质的量是 ;
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2,使其充分反应,若要使水恰好充满容器,理论上需要参加反应的O2的物质的量是多少摩尔?(计算过程)
化学对人体健康和人类生活有着十分重要的作用。请回答下列问题:
(1)抗胃酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质。抗胃酸药物具有抗酸作用的原因是_____________________________________。某品牌抗酸药的主要成分有糖衣、碳酸氢钠、氢氧化铝、淀粉。写出该抗酸药发挥功效时的离子方程式:________________________________、_______________________________。
(2)甲同学患了夜盲症,可能的原因之一是体内缺少维生素 (A、B、C、D,下同);乙同学在刷牙时牙龈经常出血,该同学在平时应多吃富含维生素 食物。
(3)铝的金属活动性比较强,铝在空气中却比较稳定,其原因是
(4)为了改善空气质量,必须控制二氧化硫氮氧化物烟尘等污染物的排放量,对汽车加装尾气催化净化装置,可使其中的NO和CO转化为无毒气体,该反应的化学方程式为 。
NO、NO2、NH3、SO2、CO等都是空气污染物。
(1)酸雨的形成主要是大气中的_________溶于水后形成了酸性溶液。
(2)在汽车的排气管上装一个催化转化装置,可使汽车尾气中的NO与CO反应,生成氮气和碳的另一种无污染的气体,请完成该转化的化学方程式: NO + CO—N2+ 。
除去下表内各物质中含有的少量杂质,写出除杂试剂,并填写分离方法。
| 序号 |
物质 |
杂质 |
所加试剂 |
分离方法 |
| (1) |
NO |
NO2 |
|
|
| (2) |
Fe粉 |
Al粉 |
|
|
| (3) |
氯化钠固体 |
氯化铵固体 |
|
|
汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物:CmHn(烃)、SO2、NOx、CO和C等,请回答下列有关问题:
(1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为________________,汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由________能转化为________能,最终转化为机械能;
(2)通过车用燃油的精炼加工处理,可减少汽车尾气中的__________(填化学式,多填本空不得分)排放;
(3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下NOX与CO反应的化学方程式________。
次磷酸H3PO2是一种强还原剂,将它加入CuSO4水溶液,加热到40~50℃,析出一种红棕色的难溶物A。经鉴定:反应后的溶液是磷酸和硫酸的混合物;X射线衍射证实A中各元素的原子个数相等;A的主要化学性质如下:
①温度超过60℃,分解成金属铜和一种气体;
②在氯气中着火;
③与盐酸反应放出气体。
(1)A的化学式为
(2)A的生成反应方程式为
(1)在中学所学的金属单质中,在冷的浓硫酸或硝酸中会发生钝化现象的有_______(填化学式);
(2)写出铁与浓硫酸(足量)在加热条件下反应的化学方程式___________________;
(3)铝分别与氢氧化钠溶液和稀硫酸反应,若在相同情况下得到相同体积的气体,则两个反应中消耗氢氧化钠与硫酸的物质的量之比为___________。
(13分)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C ②C+F→D ③D+NaOH F+E+H2O
F+E+H2O
(1)写出它们的化学式:A________、B________、C________、D________、E________、F________;
(2)写出各步反应的化学方程式,并指出反应①的氧化剂和还原剂。
①________________________,氧化剂________、还原剂________。
②________________________。
③________________________。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式________________________。
【化学—选修2:化学与技术】(15分)
I、污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀。下列物质不能作为沉淀剂的是
| A.氨水 | B.硫化氢气体 | C.硫酸钠溶液 | D.纯碱溶液 |
II、合成氨的流程示意图如下:
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是 , ;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式 ,
;
(2) 设备A中含有电加热器、触煤和热交换器,设备A的名称 ,其中发生的化学反应方程式为 ;
(3) 设备B的名称 ,其中m和n是两个通水口,入水口是 (填“m”或“n”)。不宜从相反方向通水的原因 ;
(4) 设备C的作用 ;
(5)在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g) CO2 (g)+ H2 (g) , 已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于 。
CO2 (g)+ H2 (g) , 已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于 。
试题篮
()