一定条件下,中学化学常见物质甲、乙之间存在如下转化关系,乙是
| A.HCl | B.FeCl2 | C.KOH | D.NaHCO3 |
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 |
实验 |
现象 |
结论 |
| A. |
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 |
有气体生成,溶液呈血红色 |
稀硝酸将Fe氧化为Fe3+ |
| B. |
将铜粉加1.0mol·L-1Fe2(SO4)3溶液中 |
溶液变蓝、有黑色固体出现 |
金属铁比铜活泼 |
| C. |
用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 |
熔化后的液态铝滴落下来 |
金属铝的熔点较低 |
| D. |
将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 |
现有白色沉淀生成后变为浅蓝色沉淀 |
Cu(OH)2的溶度积比Mg(OH)2的小 |
根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为: NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.从能量角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D.从第③步到第④步的目的是为了浓缩富集溴 |
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol/L的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是: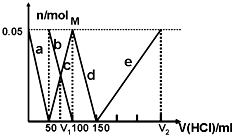
| A.原混合溶液中的CO2-3与AlO-2的物质的量之比为1:2 |
| B.V1:V2=1:5 |
| C.M点时生成的CO2为0.05mol |
| D.a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓ |
已知X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是
(甲)XO3n+Xn+H+--X单质+H2O(未配平);(乙)Mm++mOH-→M(OH)m↓
①若n=1,则XO3n中X元素为+5价,X位于周期表第VA族
②若n=2.则X最高价氧化物的水化物可能与它的氢化物反应
③若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
④若m=3,则MCl3与氢氧化钠溶液互滴时的现象可能不同
| A.②③ | B.②④ | C.①② | D.①③ |
将2aL Al2(SO4)3和(NH4)2SO4的混合溶液分成两等份,其中一份加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀;另一份加入足量强碱并加热可得到c mol NH3,则原混合溶液中的Al3+离子浓度(mol/L)为( )
A. |
B. |
C. |
D. |
根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2.24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
将1.52 g铜镁合金完全溶解于50 mL密度为1.40 g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL (标准状况),向反应后的溶液中加入浓度为1.0 mol·L-1的 NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀,下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是16∶3 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol·L-1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.反应中转移电子的物质的量为0.06 mol |
有一种混合气体,它可能由CO、CO2、SO2、HCl中的一种或多种气体组成。该气体依次通过下列物质的现象如下:通过一定量的澄清石灰水无白色沉淀析出;通过品红溶液,溶液红色褪去;通过炽热的CuO,固体变为红色;通过澄清石灰水,出现白色沉淀。该混合气体组成的各说法中,正确的是
| A.肯定不含有CO2 |
| B.只含有SO2和CO |
| C.含有SO2、CO和CO2,可能含HCl |
| D.含HCl、SO2和CO,可能含CO2 |
将一定量的Fe、Fe2O3、 CuO的混合物放入体积为100 mL、浓度为2.2 mol·L-1的H2SO4溶液中,充分反应后,生成气体896mL(标况),得到不溶固体1.28 g,过滤后,滤液中的金属离子只有Fe2+(假设滤液体积仍为100mL)。向滤液滴加2 mol·L-1的 NaOH溶液至40mL时开始出现沉淀。则未滴加NaOH溶液前滤液中FeSO4的物质的量浓度为
| A.1.6mol·L-1 | B.1.8mol·L-1 | C.2.0mol·L-1 | D.2.2mol·L-1 |
有序思维模式有利于解决复杂混合体系中的化学问题。下列反应先后顺序判断正确的是
| A.在含等物质的量的CO32-、OH-的溶液中,逐滴加入稀盐酸: OH-、CO32-、HCO3- |
| B.在含等物质的量的Al3+、NH4+的溶液中,逐滴加入NaOH溶液: Al3+、Al(OH)3、NH4+ |
| C.在含铁和铜的混合物中逐滴加入稀硝酸:Fe、Cu、Fe2+ |
| D.惰性电极电解含等物质的量Zn2+、Al3+溶液时阴极电极反应:Zn2+、Al3+、H+ |
甲、乙、丙、丁是原子序数依次增大的四种短周期元素,A、B、C、D、E是由其中的两种或三种元素组成的化合物,F是由丙元素形成的单质。已知:A+B=D+F,A+C=E+F; 0.1mol•L-1D溶液的pH为13(25℃).下列说法正确的是
A.原子半径:丁>丙>乙>甲
B.1mol A与足量B完全反应共转移了2mol电子
C.丙元素在周期表中的位置为第二周期第ⅣA族
D.由甲、乙、丙、丁四种短周期元素组成的盐,其水溶液既有呈酸性的,也有呈碱性的
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0 mol•L-1的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
| A.Cu与Cu2O的物质的量之比为2:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
下列有关的计算分析不正确的是( )
| A.在反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O中,当有1 mol铜被氧化时,被还原的硝酸为2/3mol |
| B.将a mol硫化亚铁放入含3a mol H2SO4的浓硫酸中,充分反应后,氧化、还原产物分别是Fe3+、S和SO2,则放出的气体少于1.5a mol |
| C.室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧。则a、b的关系为a=4b+3c |
| D.某溶液100 mL,其中含硫酸0.03 mol,硝酸0.04 mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015 mol |
试题篮
()