(6分)开发新型储氢材料是氢能利用的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的未成对电子数有______个。
②LiBH4由Li+和BH4-构成,BH4-呈正四面体构型。LiBH4中不存在的作用力有______(填标号)。
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为______。
(2) 金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+______H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是______(填元素符号)。
(3)某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有______种。
下列说法正确的是
| A.π键是由两个p轨道“头碰头”重叠形成的 |
| B.σ键就是单键,π键就是双键 |
| C.乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键 |
| D.H2分子中含σ键,而Cl2分子中含π键 |
CO2的资源利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应(未配平):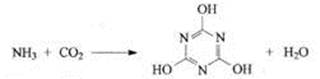
下列有关三聚氰酸的说法正确的是
| A.分子式为C3H6N3O3 | B.分子中既含极性键,又含非极性键 |
| C.属于共价化合物 | D.生成该物质的上述反应为中和反应 |
对下列化学用语的理解正确的是( )
A.原子结构示意图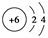 :可以表示12C,也可以表示14C :可以表示12C,也可以表示14C |
B.比例模型 :可以表示二氧化碳分子,也可以表示水分子 :可以表示二氧化碳分子,也可以表示水分子 |
C.电子式: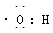 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
| D.分子式C2H4O2:可以表示乙酸,也可以表示乙二醇 |
下列物质中既存在共价键又离子键的是
| A.Na2O2 | B.MgCl2 | C.SiO2 | D.H2SO4 |
下列化合物中,既含有离子键又含有共价键的是
| A.BaCl2 | B.H2O | C.Ca(OH)2 | D.Na2O |
下列各组物质中化学键的类型相同的是( )
| A.HCl MgCl2 NH4Cl | B.H2O Na2O CO2 |
| C.CaCl2 NaOH H2S | D.NH3 H2O CO2 |
下列说法正确的是( )
| A.含有共价键的化合物一定是共价化合物 |
| B.分子中只有共价键的化合物一定是共价化合物 |
| C.离子键就是阴、阳离子间相互吸引 |
| D.只有非金属原子间才能形成共价键 |
下列变化中,吸收的热量用于克服分子间作用力的是
| A.加热金属铝使之熔化 |
| B.加热金刚石使之熔化 |
| C.液溴受热变成溴蒸气 |
| D.加热碘化氢使之分解 |
下列物质中,只含有共价键的是
| A.Na2O | B.NaCl | C.HCl | D.NaOH |
试题篮
()