下列既含离子键又含有极性键的物质是
| A.NaCl | B.NaOH | C.H2 | D.HC1 |
CoCl3·4NH3用H2SO4溶液处理再结晶,SO42—可以取代化合物中的Cl—,但NH3的含量不变,用过量的AgNO3处理该化合物,有含量1/3氯以AgCl析出,这种化合物应该是
| A.[Co(NH3)4] Cl3 | B.[Co(NH3)4 Cl3] |
| C.[Co(NH3)4 Cl] Cl2 | D.[Co(NH3)4 Cl2] Cl |
下列叙述中正确的是
| A.冰融化时水分子中共价键发生断裂 |
| B.H2O2、PCl5都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的酸性依次增强 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
下列各项中表达正确的是
A.NaCl的电子式: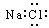 |
B.CO2的分子模型示意图: |
C.CrO5的结构式为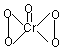 ,该氧化物中Cr为+6价 ,该氧化物中Cr为+6价 |
| D.次氯酸的结构式:H-Cl-O |
下列说法错误的是( )
| A. |
糖类化合物也可称为碳水化合物 |
| B. |
维生素D可促进人体对钙的吸收 |
| C. |
蛋白质是仅由碳、氢、氧元素组成的物质 |
| D. |
硒是人体必需的微量元素,但不宜摄入过多 |
下列各项表述正确的是
A.羟基的电子式 |
| B.醛基官能团符号-COH |
| C.乙醇的分子式:CH3CH2OH |
| D.异丁烷的结构简式: CH3CH(CH3)CH3 |
膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,它的分子是三角锥形。以下关于PH3的叙述中,正确的是
| A.PH3是非极性分子 |
| B.PH3分子中有未成键的电子对 |
| C.PH3是强氧化剂 |
| D.PH3分子中的P—H键是非极性键 |
下列物质中含有共价键的离子化合物是
| A.HCl | B.NaOH | C.CaCl2 | D.N2 |
下列分子中所有原子都满足最外层8电子结构的是( )
①CO2 ②XeF6 ③PCl3 ④SO2 ⑤BF3 ⑥N2 ⑦P4 ⑧PCl5
| A.①③⑥⑦ | B.①④⑤ | C.①④⑥ | D.②③④⑤ |
化学式为N2H6SO4的某晶体,其晶体类型与硫酸铵相同,则N2H6SO4晶体中不存在
| A.离子键 | B.共价键 | C.分子间作用力 | D.阳离子 |
用VSEPR理论预测BF3和NF3的立体结构,两个结论都正确的是
| A.平面三角形;平面三角形 | B.平面三角形;三角锥形 |
| C.平面三角形;正四面体 | D.直线形;三角锥形 |
食盐、食醋、黄酒、蔗糖、淀粉等均为家庭厨房常见的物质,下列有关说法或化学用语的表示正确的是
A.食盐中氯化钠的电子式: |
| B.蔗糖分子与食醋中的醋酸分子的最简式相同 |
| C.黄酒中乙醇的结构简式:CH3CH2OH |
| D.淀粉在一定条件下水解的最终产物是蔗糖 |
试题篮
()