运用有关概念判断下列说法正确的是
| A.NH4Cl中有离子键,是离子化合物 |
| B.46g C2H5OH燃烧放出的热量为乙醇的燃烧热 |
C.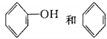 互为同系物 互为同系物 |
| D.绿色化学的核心是应用化学原理对环境污染进行治理 |
下列说法正确的是
| A.含有共价键的化合物一定是共价化合物 |
| B.KI和HI中化学键类型完全相同 |
| C.Na2O2中既含有离子键又含有非极性共价键 |
| D.NH4Cl中只含有共价键 |
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
下列说法中正确的是
| A.CO和O生成CO2是吸热反应 |
| B.在该过程中,CO断键形成C和O |
| C.CO和O生成了具有极性共价键的CO2 |
| D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 |
下列说法中正确的是
| A.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| B.同主族元素形成的氧化物的晶体类型均相同 |
| C.全部由极性键构成的分子一定是极性分子 |
| D.分子晶体中都存在范德华力,可能不存在共价键 |
下列性质与氢键无关的是
| A.NH3的熔、沸点比第ⅤA族其他元素氢化物的熔、沸点高 |
| B.乙酸可以和水以任意比互溶 |
| C.常温下H2O为液态,而H2S为气态 |
| D.水分子高温下也很稳定 |
下列变化过程中,只破坏共价键的是
| A.HCl溶于水得盐酸 | B.NaCl颗粒被粉碎 |
| C.I2升华 | D.NH4Cl晶体加热分解 |
下列各项中,理由、结论及因果关系均正确的是
| 选项 |
理由 |
结论 |
| A |
键能:N≡N>Cl-Cl |
单质沸点:N2>Cl2 |
| B |
分子中可电离的H+个数:H2SO4>CH3COOH |
酸性:H2SO4>CH3COOH |
| C |
元素的金属性:K>Na |
碱性:KOH>NaOH |
| D |
氧化性:Fe3+>Cu2+ |
还原性:Fe2+>Cu |
σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成。则下列分子中的σ键是由两个原子的s、p轨道以“头碰头”方式重叠构建而成的是
| A.H2 | B.Cl2 | C.NaH | D.HF |
下列说法错误的是( )
| A. |
糖类化合物也可称为碳水化合物 |
| B. |
维生素D可促进人体对钙的吸收 |
| C. |
蛋白质是仅由碳、氢、氧元素组成的物质 |
| D. |
硒是人体必需的微量元素,但不宜摄入过多 |
膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,它的分子是三角锥形。以下关于PH3的叙述中,正确的是
| A.PH3是非极性分子 |
| B.PH3分子中有未成键的电子对 |
| C.PH3是强氧化剂 |
| D.PH3分子中的P—H键是非极性键 |
下列物质中含有共价键的离子化合物是
| A.HCl | B.NaOH | C.CaCl2 | D.N2 |
下列分子中所有原子都满足最外层8电子结构的是( )
①CO2 ②XeF6 ③PCl3 ④SO2 ⑤BF3 ⑥N2 ⑦P4 ⑧PCl5
| A.①③⑥⑦ | B.①④⑤ | C.①④⑥ | D.②③④⑤ |
化学式为N2H6SO4的某晶体,其晶体类型与硫酸铵相同,则N2H6SO4晶体中不存在
| A.离子键 | B.共价键 | C.分子间作用力 | D.阳离子 |
下列物质中,存在非极性键的化合物的是
| A.NaOH | B.CH4 | C.H2 | D.Na2O2 |
试题篮
()