20世纪90年代,国际上提出了“预防污染”的根本手段发展“绿色化学”,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各环节都能实现净化和无污染的反应途径。下列各项属于“绿色化学”的是( )
| A.处理废弃物 |
| B.治理污染点 |
| C.减少有毒源 |
| D.杜绝污染源 |
丁香油酚的结构简式是 ,该物质不应有的化学性质是( )
,该物质不应有的化学性质是( )
①可以燃烧 ②可以跟溴加成 ③可以将酸性KMnO4溶液还原 ④可以跟NaHCO3溶液反应 ⑤可以跟NaOH溶液反应 ⑥可以发生消去反应
| A.①③ | B.③⑥ | C.④⑤ | D.④⑥ |
卤代烃在氢氧化钠存在的条件下水解,这是一个典型的取代反应,其实质是带负电的原子团(例如OH-等阴离子)取代卤代烃中的卤原子。例如:
CH3CH2CH2Br+OH-(或NaOH) CH3CH2CH2—OH+Br-(或NaBr)
CH3CH2CH2—OH+Br-(或NaBr)
写出下列反应的化学方程式:
(1)溴乙烷跟NaHS反应______________________________________________________。
(2)碘甲烷跟CH3COONa反应_________________________________________________。
(3)由碘甲烷、无水乙醇和金属钠合成甲乙醚(CH3—O—CH2CH3)。_______________。
2002年9月4日南京汤山发生了一起震惊全国的特大投毒案,犯罪分子在食品中投入了毒鼠剂——毒鼠强,导致多人中毒死亡;已知毒鼠强的结构简式如下图,有关毒鼠强(化学名:四亚甲基二砜四胺)的下列说正确的是…( )
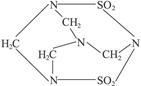
| A.毒鼠强属于无机物 |
| B.毒鼠强属于烃 |
| C.毒鼠强分子内含SO2分子因而具有毒性 |
| D.毒鼠强的分子式为C4H8N4S2O4 |
可用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是( )
| A.氯化铁溶液,溴水 |
| B.碳酸钠溶液,溴水 |
| C.高锰酸钾酸性溶液,溴水 |
| D.高锰酸钾酸性溶液,氯化铁溶液 |
下列说法正确的是( )
| A.纯净的苯酚是粉红色晶体,65 ℃以上能与水互溶 |
| B.苯中混有少量苯酚,可先加适量浓溴水,再过滤可以将苯酚除去 |
| C.苯酚的酸性可通过苯酚能与氢氧化钠反应来证明 |
| D.苯酚应密封保存,且要在上面加水以防苯酚挥发 |
丁香油酚是一种液体,它的结构简式为 ,丁香油酚不应具有的化学性质是( )
,丁香油酚不应具有的化学性质是( )
| A.可燃烧 |
| B.可使KMnO4酸性溶液褪色 |
| C.可与溴水发生加成反应 |
| D.可与NaHCO3溶液反应放出CO2 |
下列事实:①甲苯能使KMnO4(H+)溶液褪色而乙烷不能;②甲醛能发生银镜反应而甲醇不能;③苯酚分子中的羟基酸性比乙醇分子中的羟基酸性强。可以说明有机物分子中的原子间(或原子与原子团之间)的相互影响会导致物质化学性质不同的是( )
| A.只有①③ | B.只有①② | C.只有②③ | D.①②③ |
一定温度下,W g下列物质在足量氧气中充分燃烧,产物与过量的Na2O2完全反应,Na2O2固体增重W g,符合此要求的组合是( )
①H2 ②CO ③CO和H2 ④HCOOCH3⑤HOOC—COOH
| A.全部 | B.仅④⑤ | C.仅①②③ | D.除⑤外 |
中草药素皮中含有的七叶树内酯 (碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别是( )
(碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别是( )
| A.3 mol,2 mol | B.3 mol,4 mol | C.2 mol,3 mol | D.4 mol,4 mol |
分子式为CxHyO2的有机化合物1 mol在氧气中完全燃烧后,生成二氧化碳与水蒸气的体积相等(同温同压),并消耗氧气3.5 mol。则x、y的值分别是( )
| A.1,2 | B.2,4 | C.3,6 | D.4,8 |
某有机化合物的氧化产物甲、还原产物乙都能与钠反应放出氢气,甲、乙在浓硫酸催化下反应生成丙,丙能发生银镜反应,这种有机化合物是( )
| A.甲酸 | B.甲醛 | C.甲醇 | D.甲酸甲酯 |
试题篮
()